Activeer eens een C–H binding: de platina-gekatalyseerde vorming van eindstandige alcoholen uit alkanen in azijnzuur als reactiesolvent
De activatie van koolstof-waterstofbindingen (C–H) is een aangewezen methode voor de valorisatie van alkanen, omdat zij toelaat in één stap en met minder afval nuttige componenten te vormen uit deze doorgaans weinig reactieve verbindingen. In het bijzonder vormt de directe omzetting van alkanen tot lineaire, eindstandige alcoholen een aantrekkelijke route, maar vooralsnog bestaat zo’n proces niet op industriële schaal. In deze masterproef werd een proof of concept geleverd voor de platina-gekatalyseerde omzetting van langere alkanen (m.n. n-heptaan) tot het corresponderende alcohol in azijnzuur als reactiemidden.
De directe hydroxylatie van alkanen is een “schone” reactie …
Jaarlijks worden zo’n 330 miljoen ton chemicaliën geproduceerd, waarvan het grootste deel (ca. 280 miljoen ton) nog steeds van fossiele oorsprong is. In het bijzonder bestaan aardolie en aardgas voor een belangrijke fractie uit alkanen. Dankzij hun wereldwijde beschikbaarheid, gecombineerd met een gunstige prijs, vormen alkanen een aantrekkelijk uitgangsmateriaal voor de synthese van allerhande chemicaliën. Omdat ze al een alifatische keten bevatten (die enkel uit koolstof- en waterstofatomen opgebouwd is), zijn ze uitermate geschikt voor de synthese van lineaire, eindstandige alcoholen (waarbij op het uiteinde van de keten één waterstofatoom (H) door een zuurstofhoudende (O) hydroxylgroep (OH) vervangen is). Op basis van deze moleculen, met een jaarlijkse productie van 3,1 miljoen ton (2015), wordt een brede waaier aan detergenten, geurstoffen en weekmakers vervaardigd. Idealiter is het zuurstofatoom finaal afkomstig van moleculaire zuurstof (O2), omdat O2 goedkoop en abundant beschikbaar is en met het gebruik ervan als oxidans geen nevenproducten (m.u.v. water) gepaard gaan. Bovendien is de directe hydroxylatie thermodynamisch gunstig, daar ze exergonisch is (er komt energie vrij in de reactie).
… maar vereist een katalysator
Door de sterke koolstof-waterstofbindingen zijn alkanen echter weinig reactief en tot op heden ontbreekt een grootschalig proces voor de rechtstreekse hydroxylatie tot de gewenste alcoholen. Bijgevolg is de petrochemische industrie nog steeds aangewezen op energie- en kostenintensieve meerstapsprocessen. Als oplossing voor deze problematiek, wordt naarstig gezocht naar uiteenlopende methoden om de sterke C–H bindingen te activeren, d.w.z. ze te verzwakken om ze uiteindelijk te breken. Een veelbelovende strategie is activatie m.b.v. elektrofiele transitiemetalen, bijv. platina (Pt) of palladium (Pd). Deze metalen fungeren als katalysator in de reactie, d.w.z. dat ze de reactie versnellen, maar netto niet verbruikt worden. Elektrofiele transitiemetalen interageren bij voorkeur met de eindstandige C–H bindingen in het alkaan, omdat deze elektronrijk zijn en weinig ruimtelijke hinder ondervinden.
Het oudste voorbeeld hiervan is het Shilovsysteem, dat een homogene (in het reactiemidden opgeloste) Pt-katalysator (K2PtCl4, kaliumtetrachloroplatinaat) inzet voor de selectieve hydroxylatie van korte alkanen (zoals methaan) in waterig midden. De keuze van het solvent (water) beperkt de toepasbaarheid van dit systeem echter tot wateroplosbare moleculen; lange alkanen zijn daarentegen heel slecht oplosbaar in water.
Drie voordelen van azijnzuur
In deze masterproef werd het Shilovconcept geïntroduceerd in azijnzuur als reactiemidden, hetgeen drie belangrijke voordelen biedt. Allereerst wordt het substraatbereik uitgebreid naar wateronoplosbare substraten, met name langere alkanen. Daarenboven treedt verestering van de gewenste alcoholen op, wat hen resistenter maakt t.o.v. verdere oxidatie. Deze verestering werd nog begunstigd door het gebruik van een kleine hoeveelheid azijnzuuranhydride (dat meer reactief is in de verestering dan azijnzuur zelf). Ten slotte, laat de hogere oplosbaarheid van moleculaire zuurstof in azijnzuur toe om een milieuvriendelijk, abundant en goedkoop oxidans in te zetten.
Hoge selectiviteit voor het eindstandig alcohol
Als modelcomponent werd n-heptaan (Figuur 1) bestudeerd, een lineair alkaan met zeven koolstofatomen. Als eerste werd de omzetting van n-heptaan opgevolgd in functie van de tijd en de verschillende producten werden gekwantificeerd. Behalve het gewenste eindstandige alcohol (1-heptanol) werden door nevenreacties nog andere producten gevormd: zo kan ook op andere plaatsen in de koolwaterstofketen een OH-groep ingebouwd worden (dit geeft aanleiding tot 2-, 3- en 4-heptanol) en anderzijds kunnen de alcoholen zelf nog verder reageren tot ketonen, aldehyden, carbonzuren, kortere alcoholen en CO2. Niettemin werd na één uur bij 140 ºC een opmerkelijke positionele selectiviteit waargenomen: binnen de groep van de heptanolen (4 % opbrengst) gebeurde de hydroxylatie in 18 % van de gevallen op de eindstandige positie. Daarenboven werd deze waarde bereikt bij een relatief hoge omzettingsgraad (38 %) van n-heptaan. Dit staat in schril contrast met de lage positionele selectiviteit (< 2 %) en omzettingsgraad (< 5 %) die typisch bereikt worden in de conversie van alkanen onder klassieke, radicaal-gemedieerde condities.
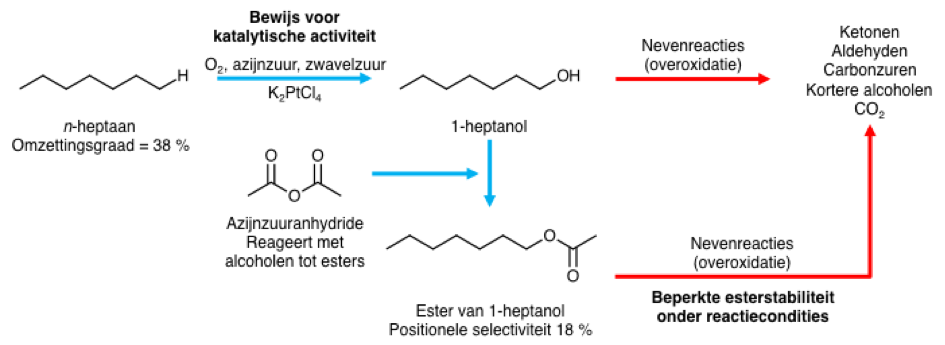
Figuur 1. Belangrijke observaties in de Pt-gekatalyseerde hydroxylatie van n-heptaan. De alifatische keten van het alkaan en alcohol wordt voorgesteld door een zigzaglijn, waarbij elk hoekpunt een C-atoom (met het bijhorend aantal H-atomen) voorstelt. De eindstandige C–H binding wordt vervangen door een C–OH binding tijdens de hydroxylatie. Het aldus gevormde alcohol reageert echter snel met azijnzuuranhydride tot het overeenkomstige ester.
In een tweede fase werd de activiteit van de Pt-katalysator bewezen. Enerzijds werd aangetoond dat het onwaarschijnlijk is dat K2PtCl4 de (radicaal-gemedieerde) nevenreacties versnelt. Zo verschilde het selectiviteitspatroon bekomen met een katalysator (kobaltdiacetaat), die de radicaal-gemedieerde reacties versnelt, zeer sterk van dat met K2PtCl4. Anderzijds werd m.b.v. een substraat dat ongevoelig is voor deze nevenreacties aangetoond dat K2PtCl4 daadwerkelijk eindstandige C–H bindingen kan functionaliseren en verantwoordelijk is voor de uitzonderlijke positionele selectiviteit.
Als laatste werd de stabiliteit van de in situ gevormde esters onderzocht. De vorming van talrijke nevenproducten gaf immers aan dat de esters onder de reactiecondities niet zo stabiel waren als initieel verondersteld werd. Mogelijk wordt de intrinsieke selectiviteit van het Shilovsysteem nog onderschat, doordat een deel van de gevormde alcoholen (beschermd als ester) in de loop van de reactie weer afgebroken wordt. Alternatieve beschermingsstrategieën werden geëvalueerd, maar verder onderzoek hieromtrent is vereist.
Toekomstperspectieven
In deze masterproef werd de toepasbaarheid van de Shilovchemie in azijnzuur voor het eerst aangetoond, waarbij een uitzonderlijke positionele selectiviteit geobserveerd werd en dit bij vrij hoge omzettingsgraad. Verdere optimalisatie van het systeem, wat betreft de productstabiliteit en reactiesnelheid, is gaande om deze vindingen te vertalen naar een directe, groene syntheseroute van eindstandige alcoholen uit langere alkanen op industriële schaal.
Dit onderzoek werd uitgevoerd aan de KU Leuven onder begeleiding van ir. Michiel Janssen en prof. dr. ir. Dirk De Vos.









