Dodelijke chronische wonden … De noodzaak voor een nieuw ontwerp voor wondverbanden
Weet u wat chronische wonden zijn? Kent u de mogelijke gevolgen? Wonden worden chronisch genoemd als deze langer dan twaalf weken aanslepen. Vaak wordt de ernst ervan onderschat en zijn de risicofactoren ongekend. Toch kunnen deze aandoeningen, wat betreft sterftecijfer, in dezelfde reeks als sommige vormen van kanker worden geplaatst. Een groter maatschappelijk besef en nieuwe behandelingen voor chronische wonden zijn een eerste stap in de goede richting.
Chronische wonden, een zwaar onderschatte aandoening
Chronische wonden worden vaak gezien als ordinaire wonden die niet genezen. Toch zijn er vaak achterliggende redenen voor. Deze wonden zijn meestal gelinkt aan andere ziektes zoals diabetes of een belemmerde bloeddoorstroming. Andere factoren die een rol kunnen spelen zijn een verzwakt immuunsysteem, ondervoeding, chronische mechanische druk, leeftijd en een verminderde mobiliteit (denk maar aan ouderen met doorligwonden).
Chronische wonden zijn verantwoordelijk voor een gigantische economische kost voor de maatschappij. Zo wordt geschat dat drie tot zes procent van de uitgaven voor gezondheidszorg toegewezen wordt aan chronische wonden. Ook zorgt deze aandoening voor een zware psychologische last voor de patiënten. Immobiliteit, werkloosheid en sociale isolatie zijn hierbij factoren die het genezingsproces extra bemoeilijken.
Zijn er dan geen beschikbare behandelingen?
De ontwikkeling van behandelingen voor chronische wonden verloopt vaak traag en moeizaam, mede door het gebrek aan publieke belangstelling. Verder wordt verzorging bemoeilijkt door het feit dat elke wonde en elke patiënt anders is. Er is immers geen universele behandeling voor chronische wonden. Ondanks deze drempel zijn er verschillende behandelingen. Deze kunnen gaan van wondverbanden over vacuümgeassisteerde wondbehandeling tot patiënt-eigen huidenten of dermale substituten.
Hoewel de huidige generatie behandelingen wel effectief zijn en vele levens redden, zijn er talrijke nadelen aan verbonden. Patiënt-eigen huidenten zijn vaak doeltreffend, maar vereisen huid van een andere plaats van het lichaam als donor. Daar kan zich dan opnieuw een chronische wonde voordoen. Dermale substituten zijn in dat opzicht een beter alternatief, maar deze bevatten vaak biologisch materiaal, waardoor het risico op afstoting niet uit te sluiten valt. Daarenboven zijn de kosten voor beide behandelingen niet te onderschatten. Vacuümgeassisteerde wondbehandeling heeft als belangrijkste nadeel dat het arbeidsintensief is, wat het kostenplaatje voor de verpleging negatief beïnvloedt. Wondverbanden kunnen een oplossing bieden, zeker indien de wonde nog niet ver “gezet” is. Er is een groot gamma aan wonderbanden beschikbaar, al dan niet specifiek gericht op chronische wonden. De ontwikkeling van nieuwe, meer performante wondverbanden met extra functionaliteiten blijft een strikte noodzaak.
Van een idee tot een eerste ontwerp
Het doel van dit thesisonderzoek was om drie concepten in de wondheling te combineren tot een nieuwe behandeling voor chronische wonden. Allereerst werd een hydrogel gebruikt als basis voor de behandeling. Dit is een materiaal dat veel water kan vasthouden en zorgt voor een vochtige wondomgeving, wat de wondheling bespoedigt.
Als tweede aspect werd “low level licht therapie” (LLLT) gebruikt. Hoewel de onderliggende mechanismen hiervan nog niet volledig achterhaald zijn, werden reeds merkwaardige resultaten behaald. Dit wordt mede toegeschreven aan de vrijgave van een molecule genaamd stikstofmonoxide (NO) in de wondomgeving. NO is een signaalmolecule en heeft zowel een antibacterieel als een anti-inflammatoir effect en reguleert de vorming van nieuwe bloedvaatjes. Echter werkt deze behandeling niet voor alle patiënten. Sommigen beschikken immers over een verminderde hoeveelheid aan NO in hun lichaam, waardoor het niet vrijgesteld kan worden door belichting.
Dit brengt ons naadloos bij het derde belangrijke luik voor het ontwikkelen van de nieuwe behandeling: het realiseren van een gecontroleerde afgifte van NO van buitenaf. Dit kan bewerkstelligd worden door het toepassen van een NO-donor (een stof waar NO zwak op gebonden is). Er zijn meerdere factoren die de vrijgave van NO van deze molecule kunnen bewerkstelligen: water, warmte en licht. Echter, het grootste nadeel aan deze NO-donoren is hun beperkte stabiliteit, voornamelijk in waterige omgeving.
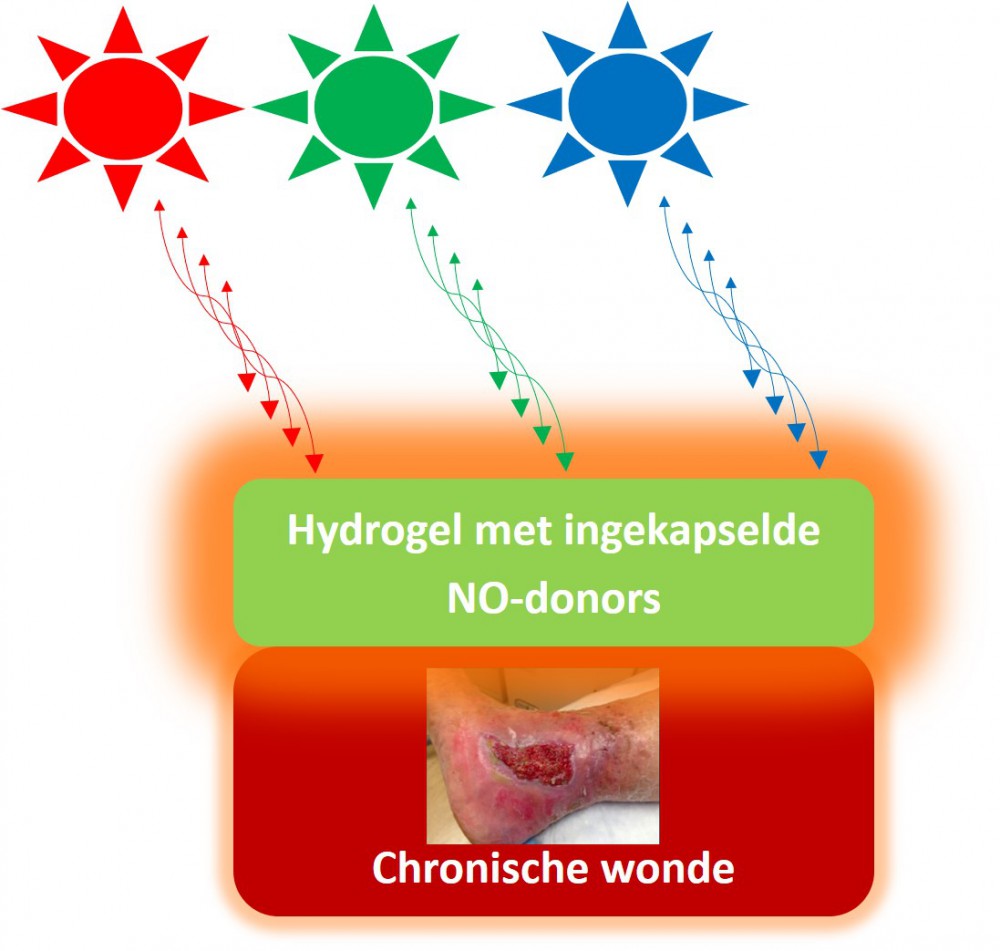
Voorgaande drie concepten werden succesvol gecombineerd tot een eerste ontwerp voor een behandeling waarbij een NO-donor ingekapseld werd in een hydrogel wondverband. LLLT kan dan gebruikt worden om zowel vanuit het lichaam zelf als van buitenaf NO vrij te geven en zo de wondgenezing te bespoedigen.
De eerste stappen …
In dit onderzoek werd in eerste instantie een totaal nieuwe, waterafstotende NO-donor gesynthetiseerd. Deze werd verondersteld een hogere stabiliteit te hebben in waterig milieu. In een vergelijking met twee commerciële NO-donoren werd besloten dat deze nieuwe NO-donor een intermediaire stabiliteit vertoont.
Verder werd de invloed van verschillende soorten licht op de vrijgave van NO getest. Hierbij toonden we aan dat blauw licht het grootste effect vertoont, gevolgd door groen licht. Bestralen van de NO-donoren met rood licht had een kleiner effect en was amper te onderscheiden van de vrijgave zonder belichting.
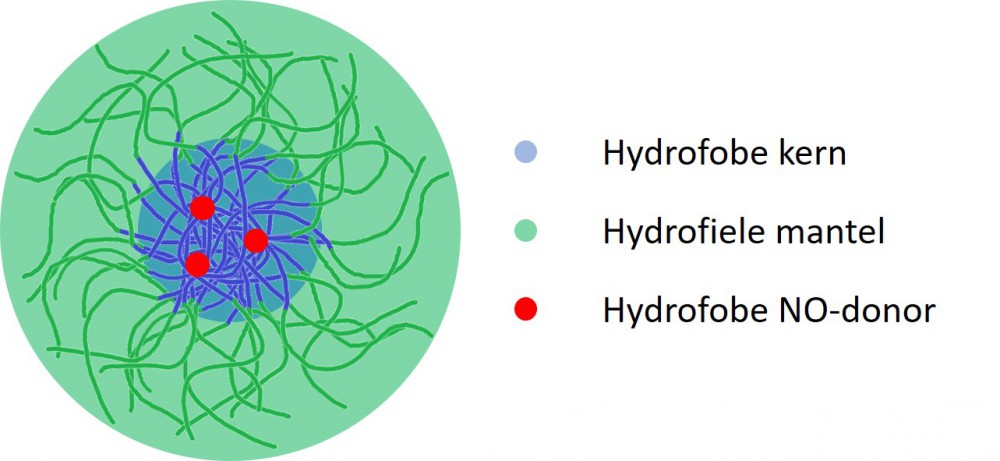
Om de stabiliteit te verhogen werd de NO-donor ook ingekapseld in een hydrogel, waarvoor Pluronic® F127 gebruikt werd. In water vormen deze moleculen micellen (capsules met een waterafstotende kern en wateroplosbare rand), waar de NO-donor in ingekapseld kan worden. De gevormde hydrogel vertoont de eigenschap dat deze van vloeibaar naar een vaste gel gaat wanneer deze warmer wordt dan 13°C. Er werd verder ook vastgesteld dat de stabiliteit van de NO-donor inderdaad verhoogd werd door inkapselen in deze hydrogel.
Ten laatste werden antibacteriële testen uitgevoerd om het effect na te gaan van de hydrogel op de groei van bacteriën. Deze resultaten toonden aan dat de hydrogel zelf een zwak antibacterieel effect vertoont, die werd aangesterkt door inkapselen van de NO-donor. Echter is het zeker nodig om verdere experimenten uit te voeren om alle positieve effecten van NO na te gaan.
Om te concluderen …
In het verrichte onderzoek werd gewerkt naar een nieuwe behandeling voor chronische wonden waarin een gecontroleerde afgifte van NO wordt gecombineerd met een hydrogel en LLLT. Hierin kan rood licht gebruikt worden om NO vrij te stellen vanuit het lichaam zelf. Wanneer het verplegende team ziet dat dit te weinig effect heeft, zou men groen of blauw licht kunnen gebruiken om van buitenaf NO toe te dienen via het wondverband. Dit onderzoek heeft ons een stap dichter gebracht naar een betere behandeling voor chronische wonden en een beter leven voor de patiënten.









