Extracellulaire vesicles als kanker biomerkers, kan het?
Kanker is een ernstige ziekte waar iedereen al wel mee in aanraking gekomen is, direct of indirect. Deze ziekte heeft een grote impact op patiënten maar ook op familieleden en vrienden. Binnen mijn thesis onderzoek werd er gefocust op de detectie optimaliseren van een gen mutatie die therapieën slecht of onwerkbaar maakt. Zo werd dus verdiept op de bruikbaarheid van een niet invasieve staal collectie methode voor mutatie opvolging in patiënten.
Mutaties opsporen in longkankers bij patiënten gebeurt momenteel door weefselbiopten af te nemen. Deze methode is invasief en garandeert niet dat er een representatieve diagnose voor de gehele tumor wordt waargenomen. Een niet-invasief alternatief zijn vloeibare biopsieën. Hiermee kunnen celvrij tumor-DNA en circulerende tumorcellen geanalyseerd worden in biologische vloeistoffen zoals het bloed. Deze zijn echter aanwezig in latere stadia van de ziekte. Daarom is er grote belangstelling voor merkers die in een vroeg stadium van kanker beschikbaar zijn, zoals extracellulaire vesicles (EVs). Deze vesicles komen vrij in de bloedbaan voor cel communicatie en bevatten dezelfde mutaties als de kankercellen waarvan ze afkomstig zijn. Het zijn een soort van pakketjes die de cel waarvan ze afkomstig zijn representeren. Deze pakketjes bevatten een dubbele membraan structuur die hun inhoud beschermt tegen kapotgaan en zo dus interessant zijn voor DNA mutatie opvolging.

In dit eindwerk wordt een methoden geoptimaliseerd om de mutatiedetectie te verbeteren van de puntmutatie T790M in het epidermale groeifactor receptor (EGFR) gen in extracellulaire vesicles afkomstig van de menselijke NCI-H1975 longkankercellijn.
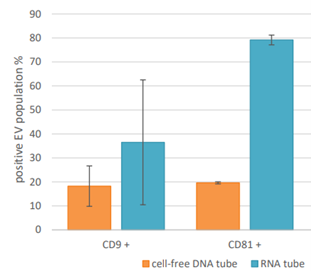
De invloed van twee verschillende bloedafnamebuisjes op de EV-concentratie in het bloed, de totale hoeveelheid proteïnen en de aanwezigheid van EV-gerelateerde proteïnemerkers werd geëvalueerd. De gebruikte RNA Complete bloedafnamebuisjes waren het best geschikt voor EV-stabilisatie. Dit is dan ook waar te nemen in onderstaande grafiek (bijgevoegde grafiek 1). CD9 en CD81 zijn proteïnen die veelvoorkomend in extracellulaire vesicles hun membranen. De populatie die deze merker bevat ligt hoger binnen het gebruikte RNA complete bloedcollectie buisje. Dit zou dus beter zijn om te gebruiken in klinische toepassingen voor EV-stabilisatie, afgewogen met wat het gewenste doel is van de EVs.
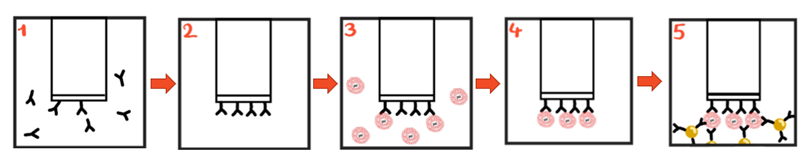
Bovendien werd bio-laaginterferometrie geoptimaliseerd voor EV-binding met NCI-H1975 cellijn afgeleide EVs die de EGFR T790M mutatie bevatten. Er werd een duidelijk negatief signaal geproduceerd door EV-binding. De conformatie van EV-binding gebeurde met behulp van een gouden nanodeeltjes sandwich essay, het verloop hiervan kan je zien aan de hand van enkele tekeningen.
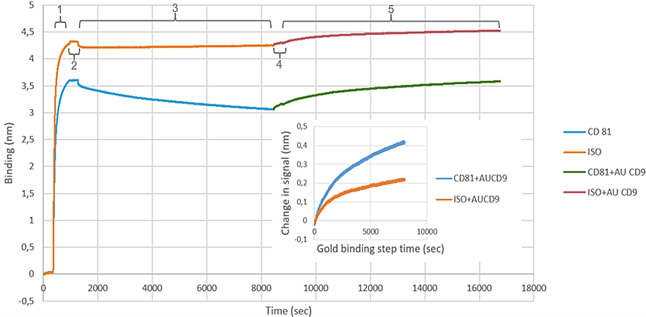
Een groter bindingssignaal verscheen bij gebruik van het anti-EV-geassocieerd proteïne CD81 antilichaam in vergelijking met het bindingssignaal van EVs bij gebruik van het anti-CD9 antilichaam. Onderzoek van de gevangen EVs gebeurden met Digitale PCR om de aanwezigheid van EGFR T790M aan te tonen. Een correlatie tussen de hoeveelheid mutaties en de gebruikte hoeveelheid EVs kon niet teruggevonden worden binnen deze proefopstellingen Dit kan verklaard worden door de aanwezigheid van vrije DNA-fragmenten die een signaal en mutatie hoeveelheid verstorende werking kunnen hebben.
Wel was er een duidelijk signaal verschil tussen te zien op de real time bio-laaginterferometrie data tussen het gebruiken van antilichamen met of zonder EVs aanwezig. Het is dus mogelijk om EVs met deze techniek te vangen.
Dit project gaf inzicht in de bruikbaarheid van EVs voor het opsporen van kankermutaties en mogelijkheden om toekomstige EV-gebaseerde moleculaire diagnostiek te verbeteren. Verdere evaluatie van een groter aantal bloedstalen en variaties tussen verschillende plasma monsters is nodig voor concrete conclusies. Wel is het al zeker, extracellulaire vesicles bieden grootse mogelijkheden voor toekomstige diagnosticering.









