Verloren hartcellen vervangen, morgen misschien wel.
- LaurensLéger
- JeffreyAalders
Elk jaar hebben miljoenen mensen wereldwijd last van een hartinfract. Bij een infarct sterven heel wat hartcellen af, waarbij die cellen niet meer te recupereren zijn. Verloren weefsel wordt dan vervangen door littekenweefsel, dat niet kan contraheren zoals de andere overblijvende hartcellen dat wel kunnen. Een deel van het hart met de bijhorende functies gaat dus verloren.
Een hogere kans op infarct
Voor een heel aantal patiënten met arrhythmogene cardiomyopathie (ACM), loopt de kans op het ontwikkelen van zulk infarct hoger dan in de normale bevolking. Er wordt geschat dat tot 1 op 5000 à 1 op 10 000 mensen jaarlijks de diagnose ACM krijgen. Dit maakt van ACM een redelijk courante ziekte, met heel wat patiënten die bij de cardioloog presenteren met hartkloppingen, ventriculaire arrhythmie (het ongewoon kloppen van een hartventrikel) en tachycardie (het te snel kloppen van het hart). Onder de microscoop bekeken, leiden ACM-patiënten van ventriculaire dilatatie (het wijder worden van een hartventrikel), een uitgedunde ventriculaire wand en de aanwezigheid van vet in het hartweefsel. Kortom, patiënten met ACM hebben een slecht functionerend hart die gevoeliger is voor het ontwikkelen van een hartinfarct.
Hartcellen in een petrischaaltje
Gelukkig zijn teams in de medische wereld bezig met het zoeken naar een oplossing voor deze patiënten. Verloren hartcellen moeten vervangen worden, maar dat is niet zo gemakkelijk. Men kan denken aan het transplanteren van een stukje hart uit een donor orgaan, maar hierbij komt het probleem van de immuunreactie optreden. Idealiter worden nieuwe hartcellen dus gemaakt vanuit de patient zelf. Een open hart operatie biedt een directe toegang tot het hart, waar de biopsie van een paar cellen kan worden genomen voor verdere kweek in het labo. Echter is zulke operatie zeer invasief en niet zonder enig risico.
Een betere oplossing is om cellen van de patiënt te nemen via een niet-invasieve methode, zoals door het schrapen van een paar wangcellen met een wattenstaafje, of door cellen die tijdens het plassen worden uitgescheiden samen met urine op te vangen. Deze cellen kunnen dan door middel van manipulatie in het labo omgezet worden tot een stamcel of moedercel, en daarna in een hartcel. De methode, voor eerst uitgevonden door prof. Yamanaka in Japan in 1995, noemt 'induced pluripotent stem cell' technologie of kortweg iPSC. Handig, want deze nieuwe hartcellen zijn genetisch identiek aan de patiënt, gezien ze van de patiënt zelf gegenereerd zijn. Een immuunreactie zal dus geen risico meer vormen bij het terug transplanteren van de cellen.
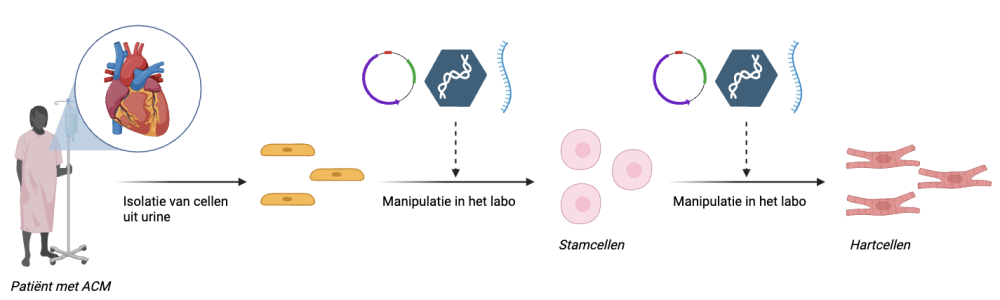
iPSC, werkelijk haalbaar?
Heel wat studies houden zich bezig met het kweken van iPSC. Het is inderdaad zo dat stamcellen, indien ze onder verschillende omstandigheden worden gekweekt, aanleiding kunnen geven tot verschillende celtypes. De iPSC methode is bijvoorbeeld dus ook toepasbaar in het milieu van de neurologie, om hersencellen die verloren gaan bij Alzheimer te vervangen.
Transplantatie van stamcel-gederiveerde cellen wordt nog niet toegepast in het ziekenhuis. Wel zijn er klinische trials met patiënten aan de gang, om de veiligheid en de reactie van iPSC's verder te onderzoeken. We komen dus elke dag een stapje dichter bij het genezen van hartinfarcten, en andere ziekten waar cellen verloren gaan.









