3D printing en MRI binden samen de strijd aan tegen prostaatkanker
Per jaar worden één miljoen mannen wereldwijd getroffen door prostaatkanker. Dit betekent dat 1 op 6 mannen prostaatkanker ontwikkelt tijdens hun leven. Prostaatkanker is bovendien de 2e dodelijkste vorm van kanker bij mannen. Met de vergrijzing van de bevolking zal dit aantal alleen nog maar stijgen. Voor de behandeling van prostaatkanker is een snelle diagnose zeer belangrijk. Daarom was deze studie gericht op de detectie van prostaatkanker in een vroeg stadium.
Waarom is een betere beeldvorming bij prostaatkanker noodzakelijk?
Op dit ogenblik wordt de diagnose voornamelijk gesteld op basis van een weefselbiopt. Dit is een pijnlijke ingreep waarbij een tiental stukjes van de prostaat worden weggenomen met een lange, fijne naald. Deze stalen worden vervolgens onderzocht op de aanwezigheid van kankercellen. Deze zeer onaangename ingreep zou kunnen vermeden worden indien de prostaat voldoende scherp in beeld kan worden gebracht met medische beeldvorming. Het doel van deze studie was om te zien of MRI beelden precies genoeg zijn om de tumoren in de prostaat te lokaliseren. Bovendien zouden patiënten met een minder agressieve vorm van kanker dan ook vaker kiezen voor het actief opvolgen van de tumor in plaats van meteen te kiezen voor een ingrijpende behandeling. Momenteel moeten er bij iedere controle opnieuw stalen worden genomen. Diagnose en opvolging op basis van MRI vergroot niet alleen het comfort van de patiënt, maar het vermindert bovendien ook nog eens de maatschappelijke kost aangezien dure behandelingen zoals robotchirurgie kunnen vermeden worden.
3D printer als hulpmiddel in klinisch onderzoek
Gedurende dit onderzoek ondergingen 14 personen, waarbij prostaatkanker werd vastgesteld, een hoge resolutie MRI scan. Daarna werd bij alle patiënten de prostaat volledig verwijderd en geanalyseerd.
Op basis van de MRI beelden werd voor iedere prostaat afzonderlijk een specifieke mal ontworpen. Deze kunststofmallen worden geproduceerd met behulp van een 3D printer. Het resultaat zijn twee helften van een cilinder in een harde kunststof waar de prostaat perfect in past. Loodrecht op de lengteas van de cilinder zijn er gleuven aanwezig in de mal. Deze gleuven maken het mogelijk om de prostaat in schijven te snijden in hetzelfde vlak als de MRI opnames. Dit ontwerp zorgt ervoor dat de MRI beelden op een correcte wijze vergeleken kunnen worden met de overeenkomstige weefselanalyses.
Resultaten van het onderzoek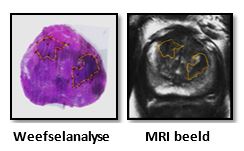
De resultaten van dit onderzoek bevestigen dat het mogelijk is om met MRI tumoren in de prostaat in beeld te brengen. Uit de analyse van deze beelden bleek dat kanker een hogere celdensiteit heeft dan gezond weefsel. Hierdoor is water in kankerweefsel minder beweeglijk. Dit is van groot belang aangezien waterstofatomen gebruikt worden om MRI beelden te vormen. Het verschil in mobiliteit van de watermoleculen laat toe om de tumoren met een hoge resolutie in beeld te brengen.
Nieuwe behandelingsstrategie van prostaatkanker in de toekomst
In tegenstelling tot de weefselbiopten die vandaag de dag worden gebruikt, is MRI een onschadelijke techniek waar de patiënt weinig ongemak van ondervindt. Dit kan ervoor zorgen dat personen vlugger de stap durven zetten om zich te laten controleren op prostaatkanker. Bovendien zorgt MRI voor een precieze lokalisatie van de tumor, wat kan helpen bij het plannen van een radiotherapie of een operatie. Zo zou het in de toekomst mogelijk moeten worden om slechts het zieke gedeelte van de prostaat te verwijderen. Op termijn kan deze techniek zelfs uitgebreid worden naar andere vormen van weefseltumoren. Dankzij de technologische vooruitgang en wetenschappelijk onderzoek zal de behandeling van prostaatkanker er in de nabij toekomst helemaal anders uitzien.
Bibliografie
1. Bray F, Lortet-Tieulent J, Ferlay J, Forman D, Auvinen A. Prostate cancer incidence and mortality trends in 37 European countries: an overview. Eur J Cancer. 2010;46(17):3040–52.
2. Miller, Rebecca L. Siegel KD, , Ahmedin Jemal D. Cancer Statistics, 2016. CA Cancer J Clin. 2016;66(1):7–30.
3. Trivedi H, Turkbey B, Rastinehad AR, Benjamin CJ, Bernardo M, Pohida T, et al. Use of patient-specific MRI-based prostate mold for validation of multiparametric MRI in localization of prostate cancer. Urology. 26;79(1):233–9.
4. Orczyk C, Mikheev A, Rosenkrantz AB, Melamed J, Taneja SS, Rusinek H. Imaging of prostate cancer: a platform for 3D co-registration of in-vivo MRI ex-vivo MRI and pathology. Proc SPIE--the Int Soc Opt Eng. 2012;8316:83162.
5. Priester A, Natarajan S, Le JD, Garritano J, Radosavcev B, Grundfest W, et al. Original Article A system for evaluating magnetic resonance imaging of prostate cancer using patient-specific 3D printed molds. Am J Clin Exp Urol. 2014;2(2):127–35.
6. Bhavsar A, Verma S. Anatomic imaging of the prostate. Biomed Res Int. 2014 Jan;2014:9.
7. Heidenreich A. New Developments in the Management of Prostate Cancer. Oncol Res Treat. 2015;38(38):628.
8. Heidenreich A, Bellmunt J, Bolla M, Joniau S, Mason M, Matveev V, et al. EAU guidelines on prostate cancer. Part 1: screening, diagnosis, and treatment of clinically localised disease. Eur Urol. 2011;59(1):61–71.
9. Date P. Incidence Fact Sheet Prostate Cancer Belgium 2013 Publication Date : 2015.
10. N. Mottet, J. Bellmunt EB, R.C.N. van den Bergh, M. Bolla, N.J. van Casteren, P. Cornford, S. Culine, S. Joniau, T. Lam, M.D. Mason, V. Matveev, H. van der Poel, T.H. van der Kwast, O. Rouvière TW. EAU-Guidelines-on-Prostate-Cancer-2015. European association of Urology. 2015.
11. Chustecka Z. Cancer Survival Rates Improving Across Europe, But Still Lagging Behind US [Internet]. Medscape medical news. 2007 [cited 2015 Nov 15]. Available from: http://www.medscape.com/viewarticle/561737
12. Bratt O. Hereditary Prostate Cancer: Clinical Aspects. J Urol. 2002;168(3):906–13.
13. OLA BRATT. Hereditary PCa. J Urol [Internet]. 2002;168:906–13. Available from: http://ac.els-cdn.com/S0022534705645417/1-s2.0-S0022534705645417-main.p…
14. Grönberg H. Prostate cancer epidemiology. Lancet. 2003;361(9360):859–64.
15. Board PATE. Prostate Cancer Treatment (PDQ®) [Internet]. National Cancer Institute (US); 2015 [cited 2015 Sep 25]. Available from: http://www.ncbi.nlm.nih.gov/books/NBK66036/
16. Thompson IM, Ankerst DP, Chi C, Goodman PJ, Tangen CM, Lucia MS, et al. Assessing prostate cancer risk: Results from the Prostate Cancer Prevention Trial. J Natl Cancer Inst. 2006;98(8):529–34.
17. Lee CH, Akin-Olugbade O, Kirschenbaum A. Overview of prostate anatomy, histology, and pathology. Endocrinol Metab Clin North Am. 2011;40(3):565–75, viii – ix.
18. Winslow T. Prostate Cancer Treatment—Health Professional Version - National Cancer Institute [Internet]. 2005 [cited 2015 Dec 10]. Available from: http://www.cancer.gov/types/prostate/hp/prostate-treatment-pdq#link/_16…
19. Wang S, Burtt K, Turkbey B, Choyke P, Summers RM. Computer Aided-Diagnosis of Prostate Cancer on Multiparametric MRI: A Technical Review of Current Research. Biomed Res Int. Hindawi Publishing Corporation; 2014;1–11.
20. Horwich A, Parker C, Bangma C, Kataja V. Prostate cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol [Internet]. 2010 May 1 [cited 2015 Aug 20];21 Suppl 5(suppl 5):v129–33. Available from: http://annonc.oxfordjournals.org/content/21/suppl_5/v129.full
21. Richenberg J, Clements R, Verma S, Villeirs G, Rouviere O, Logager V, et al. ESUR prostate MR guidelines 2012. Eur Radiol. 2012;22(4):746–57.
22. Nash PA, Bruce JE, Indudhara R, Shinohara K. Transrectal ultrasound guided prostatic nerve blockade eases systematic needle biopsy of the prostate. J Urol. 1996;155(2):607–9.
23. Nazir B. Pain during transrectal ultrasound-guided prostate biopsy and the role of periprostatic nerve block: what radiologists should know. Korean J Radiol. 2014;15(5):543–53.
24. Payne H, Cornford P. Prostate-specific antigen: an evolving role in diagnosis, monitoring, and treatment evaluation in prostate cancer. Urol Oncol.; 2009;29(6):593–601.
25. Hricak H, Scardino P. Prostate Cancer. NCCN Guidelines. 2009. p. 60.
26. Hambrock T, Hoeks C, Hulsbergen-Van De Kaa C, Scheenen T, Fütterer J, Bouwense S, et al. Prospective assessment of prostate cancer aggressiveness using 3-T diffusion-weighted magnetic resonance imaging-guided biopsies versus a systematic 10-core transrectal ultrasound prostate biopsy cohort. Eur Urol. 2012;61(1):177–84.
27. Woodfield C a., Tung G a., Grand DJ, Pezzullo J a., Machan JT, Renzulli JF. Diffusion-weighted MRI of peripheral zone prostate cancer: Comparison of tumor apparent diffusion coefficient with Gleason score and percentage of tumor on core biopsy. Int Braz J Urol. 2010;36:316–22.
29. Edge, S., Byrd, D.R., Compton, C.C., Fritz, A.G., Greene, F.L., Trotti A. AJCC Cancer Staging Manual | Stephen Edge | Springer. Seventh ed. Springer, 2010. 648 p.
30. Johnson LM, Choyke PL, Figg WD, Turkbey B. The Role of MRI in Prostate Cancer Active Surveillance. Biomed Res Int. Hindawi Publishing Corporation; 2014;1–6.
31. Dall’Era MA, Konety BR, Cowan JE, Shinohara K, Stauf F, Cooperberg MR, et al. Active surveillance for the management of prostate cancer in a contemporary cohort. Cancer. 2008;112(12):2664–70.
32. Al Otaibi M, Ross P, Fahmy N, Jeyaganth S, Trottier H, Sircar K, et al. Role of repeated biopsy of the prostate in predicting disease progression in patients with prostate cancer on active surveillance. Cancer. 2008;113(2):286–92.
33. Rider JR, Sandin F, Andrén O, Wiklund P, Hugosson J, Stattin P. Long-term outcomes
among noncuratively treated men according to prostate cancer risk category in a nationwide, population-based study. Eur Urol. 2013;63(1):88–96.
34. Bill-Axelson Anna, Holmberg Lars MR, Häggman Michael, Swen-Olof Andersson et al. Radical Prostatectomy versus Watchful Waiting in Early Prostate Cancer [Internet]. N Engl J Med. 2011 [cited 2015 Nov 15]. p. 352(19):1977–84. Available from: http://www.nejm.org/doi/pdf/10.1056/NEJMoa043739
35. De Carlo F, Celestino F, Verri C, Masedu F, Liberati E, Di Stasi SM. Retropubic, laparoscopic, and robot-assisted radical prostatectomy: surgical, oncological, and functional outcomes: a systematic review. Urol Int. 2014;93(4):373–83.
36. Borren A, Groenendaal G, Moman MR, Boeken Kruger AE, van Diest PJ, van Vulpen M, et al. Accurate prostate tumour detection with multiparametric magnetic resonance imaging: dependence on histological properties. Acta Oncol. 2014;53(1):88–95.
37. Isebaert S, Van Den Bergh L, Haustermans K, Joniau S, Lerut E, De Wever L, et al. Multiparametric MRI for prostate cancer localization in correlation to whole-mount histopathology. J Magn Reson Imaging. 2013;37(6):1392–401.
38. Akin O, Sala E, Moskowitz CS, Kuroiwa K, Ishill NM, Pucar D, et al. Transition zone prostate cancers: features, detection, localization, and staging at endorectal MR imaging. Radiology. 2006;239(3):784–92.
39. Kuru TH, Van Essen J, Pfister D, Porres D. Role of Focal Therapy with High-Intensity Focused Ultrasound in the Management of Clinically Localized Prostate Cancer. Oncol Res Treat. 2015;38:634–8.
40. Orczyk C, Rusinek H, Rosenkrantz AB, Mikheev A, Deng F-M, Melamed J, et al. Preliminary experience with a novel method of three-dimensional co-registration of prostate cancer digital histology and in vivo multiparametric MRI. Clin Radiol.;68(12):e652–8.
41. Bratan F, Niaf E, Melodelima C, Chesnais AL, Souchon R, Mège-Lechevallier F, et al. Influence of imaging and histological factors on prostate cancer detection and localisation on multiparametric MRI: A prospective study. Eur Radiol. 2013;23(7):2019–29.
42. Schild PDHH. MRI made easy. volume 1. Berlin: Schering AG; 1990. 105 p.
43. Turkbey B, Pinto P a, Mani H, Bernardo M, Pang Y, McKinney YL, et al. Prostate cancer: value of multiparametric MR imaging at 3 T for detection--histopathologic correlation. Radiology. 2010;255(1):89–99.
44. Tofts PS. T1-weighted DCE Imaging Concepts : Modelling , Acquisition and Analysis. MAGNETOM Flash. 2010;1–5.
45. Moore CM, Ridout A, Emberton M. The role of MRI in active surveillance of prostate cancer. Curr Opin Urol. 2013;23(3):261–7.
46. Westphalen AC, Coakley F V, Kurhanewicz J, Reed G, Zhen J, Simko JP. Spectroscopy Features. AJR Am J Roentgenol. 2010;193(3):238–43.
47. Bourne R, Kurniawan N, Cowin G, Sved P, Watson G. 16 T Diffusion microimaging of fixed prostate tissue: Preliminary findings. Magn Reson Med. 2011;66(1):244–7.
48. Oto A, Yang C, Kayhan A, Tretiakova M, Antic T, Schmid-Tannwald C, et al. Diffusion-weighted and dynamic contrast-enhanced MRI of prostate cancer: Correlation of
quantitative MR parameters with gleason score and tumor angiogenesis. Am J Roentgenol. 2011;197(6):1382–90.
49. Miao H, Fukatsu H, Ishigaki T. Prostate cancer detection with 3-T MRI: comparison of diffusion-weighted and T2-weighted imaging. Eur J Radiol. 2007;61(2):297–302.
50. Weinreb JC, Barentsz JO, Choyke PL, Cornud F, Haider MA, Macura KJ, et al. PI-RADS Prostate Imaging - Reporting and Data System: 2015, Version 2. Eur Urol [Internet]. 2015 Sep 28 [cited 2015 Oct 20];69(1):16–40. Available from: http://www.ncbi.nlm.nih.gov/pubmed/26427566
51. Shah V, Pohida T, Turkbey B, Mani H, Merino M, Pinto PA, et al. A method for correlating in vivo prostate magnetic resonance imaging and histopathology using individualized magnetic resonance-based molds. Rev Sci Instrum. 2009;80(10):104301.
52. McGrath DM, Foltz WD, Al-Mayah A, Niu CJ, Brock KK. Quasi-static magnetic resonance elastography at 7 T to measure the effect of pathology before and after fixation on tissue biomechanical properties. Magn Reson Med. 2012;68(1):152–65.
53. Chappelow J, Bloch BN, Rofsky N, Genega E, Lenkinski R, DeWolf W, et al. Elastic registration of multimodal prostate MRI and histology via multiattribute combined mutual information. Med Phys. 2011;38(4):2005–18.
54. Turkbey B, Mani H, Shah V, Rastinehad AR, Bernardo M, Pohida T, et al. Multiparametric 3T prostate magnetic resonance imaging to detect cancer: histopathological correlation using prostatectomy specimens processed in customized magnetic resonance imaging based molds. J Urol. 2011;186(5):1818–24.
55. Xiao G, Bloch BN, Chappelow J, Genega EM, Rofsky NM, Lenkinski RE, et al. Determining histology-MRI slice correspondences for defining MRI-based disease signatures of prostate cancer. Comput Med Imaging Graph.; 2011;35(7-8):568–78.
56. Chaitanya Kalavagunta, MS, MS, MSc1, Xiangmin Zhou, PhD2, Stephen C. Schmechel M, PhD3, and Gregory J. Metzger P. Registration of in vivo Prostate MRI and Pseudo-Whole Mount Histology using Local Affine Transformations guided by Internal Structures (LATIS). J Magn Reson Imaging. 2015;73(4):389–400.
57. Orczyk, Clement, Taneja Samir S, Rusinek Henry RAB. Assessement of Change in Prostate Volume and Shape Following Surgical Resection Through Co-registration of In Vivo MRI and Fresh Specimen Ex Vivo MRI. Clin Radiol. 2015;2(2):398–403.
58. Fomby P, Cherlin AJ. Challenges in accurate registration of 3D medical imaging and histopathology in primary prostate cancer. Eur J Nucl MEd Mol Imaging. 2011;72(2):181–204.
59. Delongchamps NB, Rouanne M, Flam T, Beuvon F, Liberatore M, Zerbib M, et al. Multiparametric magnetic resonance imaging for the detection and localization of prostate cancer: Combination of T2-weighted, dynamic contrast-enhanced and diffusion-weighted imaging. BJU Int. 2011;107(9):1411–8.
60. Vanden Berghe S. Assessment of Prostate Tumors using High Resolution In Vivo and Ex Vivo MRI. 2016.
61. Haider MA, van der Kwast TH, Tanguay J, Evans AJ, Hashmi A-T, Lockwood G, et al. Combined T2-Weighted and Diffusion-Weighted MRI for Localization of Prostate Cancer. Am J Roentgenol. American Roentgen Ray Society; 2007;189(2):323–8.
62. Xiao G, Bloch BN, Chappelow J, Genega EM, Rofsky NM, Lenkinski RE, et al. Determining histology-MRI slice correspondences for defining MRI-based disease signatures of prostate cancer. Comput Med Imaging Graph; 2011;35(7-8):568–78.
63. Uribe CF, Jones EC, Chang SD, Goldenberg SL, Reinsberg SA, Kozlowski P. In vivo 3T and ex vivo 7T diffusion tensor imaging of prostate cancer: Correlation with histology. Magn Reson Imaging. 2015 Jun;33(5):577–83.
64. Chatterjee A, Watson G, Myint E, Sved P, McEntee M, Bourne R. Changes in epithelium, stroma, and lumen space correlate more strongly with gleason pattern and are stronger predictors of prostate ADC changes than cellularity metrics1. Radiology [Internet]. 2015;277(3):751–62.
65. Bourne RM, Kurniawan N, Cowin G, Sved P, Watson G. Microscopic diffusion anisotropy in formalin fixed prostate tissue: Preliminary findings. Magn Reson Med. 2012;68(6):1943–8.
66. Trivedi H, Turkbey B, Rastinehad AR, Benjamin CJ, Bernardo M, Pohida T, et al. Use of patient-specific MRI-based prostate mold for validation of multiparametric MRI in localization of prostate cancer. Urology 2012 Jan;79(1):233–9.
67. McGrath DM, Foltz WD, Brock KK. Measuring the Effect of Formalin Fixation on Ex Vivo Tissue Material Properties using High Resolution 3D Quasi-Static MR Elastography at 7 Tesla for Improved Biomechanical Registration of Histopathology , and Correlation with the Effect of Fixation on T 1. Proc Intl Soc Mag Reson Med. 2010;18:640.
68. Metrics C, Watson G. and Lumen Space Correlate More Strongly with Gleason Pattern and Are Stronger Predictors of Prostate ADC Changes than. 2015;000(0):1–12.
69. Bourne RM, Kurniawan N, Cowin G, Stait-Gardner T, Sved P, Watson G, et al. Microscopic diffusivity compartmentation in formalin-fixed prostate tissue. Magn Reson Med. 2012;68(2):614–20.
70. Bourne RM, Bongers A, Chatterjee A, Sved P, Watson G. Diffusion anisotropy in fresh and fixed prostate tissue ex vivo. Magn Reson Med. 2015 Oct 7;
71. Chen LH, Ho H, Lazaro R, Thng CH, Yuen J, Ng WS, et al. Optimum slicing of radical prostatectomy specimens for correlation between histopathology and medical images. Int J Comput Assist Radiol Surg. 2010;5(5):471–87.
72. Trivedi H, Turkbey B, Rastinehad AR, Benjamin CJ, Bernardo M, Pohida T, et al. Use of patient-specific MRI-based prostate mold for validation of multiparametric MRI in localization of prostate cancer. Urology.; 2012;79(1):233–9.
73. Elen An, Isebaert Sofie, De Keyzer Frederik, Himmelreich Uwe, Joniau Steven, Tosco Lorenzo, Dresselaers Tom, Lerut Evelyne, Oyen Raymond, Bourne Roger, Maes Frederik HK. Validation and workflow of an improved patient-specific mold design for registration of in-vivo MRI and histology of the prostate.
74. Haider MA, Van Der Kwast TH, Tanguay J, Evans AJ, Hashmi AT, Lockwood G, et al. Combined T2-weighted and diffusion-weighted MRI for localization of prostate cancer. Am J Roentgenol. 2007;189(2):323–8.
75. Bourne RM, Kurniawan N, Cowin G, Stait-Gardner T, Sved P, Watson G, et al. Biexponential diffusion decay in formalin-fixed prostate tissue: Preliminary findings. Magn Reson Med. 2012;68(3):954–9.
76. Fan X, Haney CR, Agrawal G, Pelizzari CA, Antic T, Eggener SE, et al. High-resolution MRI of excised human prostate specimens acquired with 9.4T in detection and identification of cancers: validation of a technique. J Magn Reson Imaging. 2011;34(4):956–61.
77. Ferlay J, Steliarova-foucher E, Lortet-tieulent J, Rosso S. Cancer incidence and mortality patterns in Europe : Estimates for 40 countries in 2012. Eur J Cancer. 2013;49(6):1374–403.
78. Harnden P, Shelley MD, Coles B, Staffurth J, Mason MD. Should the Gleason grading system for prostate cancer be modified to account for high-grade tertiary components? A systematic review and meta-analysis. Lancet Oncol.; 2007;8(5):411–9.









