Kwallen bij de vis, een extra druk op Noorse fjorden
- AnnVanreusel
Noorwegen is al decennialang de wereldleider in de productie van gekweekte zalm. De laatste jaren kennen de Noorse fjorden echter ook een toename in een ander organisme: Periphylla periphylla, een rode en lichtgevende schijfkwal. Het is een geduchte concurrent voor de wilde vissen, maar ook dood kan het dier blijkbaar nog problemen opleveren.
Centrum van de aquacultuur
In 2016 produceerde Noorwegen nog meer dan 1,3 miljoen ton aan gekweekte vis, waarvan 93% zalm. Etensresten en uitwerpselen afkomstig van de viskwekerijen verrijken plaatselijk de zeebodem, wat tot veranderingen in dat ecosysteem leidt. De Noorse zalmindustrie produceert even veel stikstof als er in het onbehandeld rioolwater van 3,9 miljoen mensen zit. De kwekerijen bevinden zich in diepe zones van de fjord, waardoor de afvalstoffen over een groot oppervlak worden verspreid en zo de plaatselijke druk op de zeebodem wordt verlicht. Toch is hun effect in de gewoonlijk voedselarme fjorden nog steeds merkbaar; het zuurstofgehalte in de bodem daalt door een verhoogde activiteit van microben en de diversiteit aan bodemorganismen wordt kleiner, doordat slechts enkele soorten onder deze lastige omstandigheden kunnen overleven.
Een nieuwe speler
P. periphylla, ook wel de helmkwal genoemd naar zijn vorm, is een diepwatersoort die de laatste jaren enorm in aantal is toegenomen in Noorse fjorden. Niet alleen is het eigenlijk een toppredator, die zowel het voedsel als het nageslacht van concurrenten zoals kabeljauw en schelvis eet, maar de voortplantingssnelheid ligt ook hoger dan die van de meeste andere kwallen. Hierdoor bedraagt de populatie in sommige fjorden vandaag maar liefst 40.000 ton. De huidige kwallenbloei heeft in strenge winters al tot plotse massasterfte geleid, wat een extra aanvoer van voedingsstoffen in de vorm van kwalkarkassen kan betekenen. De lijkjes zakken betrekkelijk snel naar de bodem, waar ze worden afgebroken door een leger aan bodemorganismen, gaande van kreeftachtigen over wormen in alle vormen en maten tot microben. Doordat microben en kwallen overeenkomsten hebben in hun samenstelling, kunnen microben deze laatste gemakkelijker afbreken. De hoge microbiële activiteit zorgt ervoor dat het zuurstofgehalte in de bodem snel daalt, wat het leven van de rest van de gemeenschap opnieuw bemoeilijkt.
P. periphylla bij leven (L, foto: David Wrobel) en na invriezing en ontdooiing (R).
Over het effect dat de bijproducten van de viskweek hebben op de zeebodem wordt al langer onderzoek gedaan. De specifieke effecten van de kwallenlijkjes werden recentelijk pas voor het eerst onder de loep genomen. Doordat beide vormen van verrijking een verhoogde microbiële activiteit en verlaagd zuurstofgehalte tot gevolg hebben, wordt vermoed dat dit effect des te groter zou kunnen zijn in fjorden waar beide samen voorkomen.
Focus op wormen
Deze studie is de eerste die deze gecombineerde effecten in kaart wil brengen, dit door middel van een lab experiment. De bodemstalen kwamen uit regio’s met en zonder aquacultuur in de Hardangerfjord en verschillende gewichten aan dode, ontdooide kwallen werden op het oppervlak geplaatst. Echter, de sterren van dit onderzoek zijn eigenlijk niet de kwallen, maar nematoden. Dit zijn minuscule rondwormen die handig zijn in dit soort studies doordat sommige soorten het zeer goed doen in vervuilde of verrijkte bodem. In het onderzoek zagen we dat de diversiteit in de buurt van de viskwekerijen daalde en dat slechts een paar soorten in grote aantallen voorkwamen.
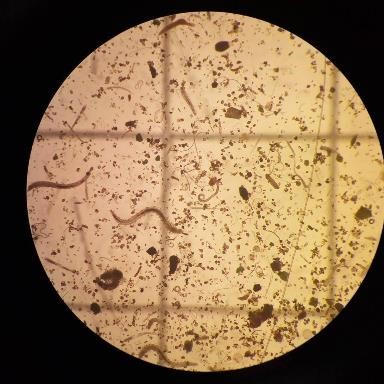
Beeld van onder het binoculair - enkel de fijne, gladde wormen zijn nematoden.
Het experimenteel toevoegen van de kwallen leidde zoals verwacht tot een duidelijk verhoogd zuurstofverbruik. In de stalen waar het meeste kwal aan was toegevoegd leek een probleem op te treden, doordat daar minder zuurstof werd verbruikt dan in de stalen met minder kwal. Het normale patroon is namelijk dat het verbruik stijgt met de hoeveelheid aan voedsel. Als de bodemorganismen het afval niet snel genoeg kunnen verwerken kan dit op de duur tot een verstoring in het ecosysteem leiden, met mogelijks verregaande gevolgen voor het leven in de fjord.
De kwallenplaag heeft dus waarschijnlijk niet enkel een invloed op al wat rondzwemt in de fjord, maar ook op het leven in de bodem. In combinatie met de nog steeds uitbreidende zalmkweek kan dit op termijn tot serieuze problemen leiden in dit voor een buitenstaander zo idyllisch ogende landschap.
Bibliografie
Aksnes, D. L., Dupont, N., Staby, A., Fiksen, Ø., Kaartvedt, S., and Aure, J. (2009). Coastal water darkening and implications for meso-pelagic regime shifts in Norwegian fjords. Marine Ecology Progress Series, 387(Jerlov 1968), 39–49. http://doi.org/10.3354/meps08120
Anderson, M. J., Gorley, R. N., and Clarke, K. R. (2008). Permanova+ for Primer: Guide to Software and Statistical Methods.
Anderson, M. J., and Robinson, J. (2003). Generalizeed discriminant analysis based on distances. Australian and New Zealand Journal of Statistics, 45(3), 301–318.
Andersson, J. H., Wijsman, J. W. M., Herman, P. M. J., Middelburg, J. J., Soetaert, K., and Heip, C. H. R. (2004). Respiration patterns in the deep ocean. Geophysical Research Letters, 31(3), 1–4. http://doi.org/10.1029/2003GL018756
Billett, D. S. M., Bett, B. J., Jacobs, C. L., Rouse, I. P., and Wigham, B. D. (2006). Mass deposition of jellyfish in the deep Arabian Sea. Limnology and Oceanography, 51(5), 2077–2083.
Bongers, T., Alkemade, R., and Yeates, G. W. (1991). Interpretation of disturbance-induced maturity decrease in marine nematode assemblages by means of the Maturity Index. Marine Ecology Progress Series, 76(2), 135–142. http://doi.org/10.3354/meps076135
Clarke, K. R., and Gorley, R. N. (2006). PRIMER V6: user manual-tutorial. Plymouth Marine Laboratory.
21
Darling, E. S., and Côté, I. M. (2008). Quantifying the evidence for ecological synergies. Ecology Letters, 11(12), 1278–1286. http://doi.org/10.1111/j.1461-0248.2008.01243.x
de Bovee, F., and Labat, J. P. (1993). A Simulation Model of a Deep Meiobenthic Compartment: A Preliminary Approach. Marine Ecology, 14(2), 159–173. http://doi.org/10.1111/j.1439-0485.1993.tb00373.x
Duplisea, D. E., and Hargrave, B. T. (1996). Response of meiobenthic size-structure , sediment organic enrichment biomass and respiration to. Hydrobiologia, 339, 161–170.
Franco, M. A., Soetaert, K., Costa, M. J., Vincx, M., and Vanaverbeke, J. (2008a). Uptake of phytodetritus by meiobenthos using 13C labelled diatoms and Phaeocystis in two contrasting sediments from the North Sea. Journal of Experimental Marine Biology and Ecology, 362(1), 1–8. http://doi.org/10.1016/j.jembe.2008.04.010
Franco, M. A., Soetaert, K., Van Oevelen, D., Van Gansbeke, D., Costa, M. J., Vincx, M., and Vanaverbeke, J. (2008b). Density, vertical distribution and trophic responses of metazoan meiobenthos to phytoplankton deposition in contrasting sediment types. Marine Ecology Progress Series, 358(Graf 1992), 51–62. http://doi.org/10.3354/meps07361
Goldman, J. C., and Dennet, M. R. (2000). Growth of marine bacteria in batch and continuous culture under carbon and nitrogen limitation. Limnology and Oceanography, 45(4), 789–800. http://doi.org/10.4319/lo.2000.45.4.0789
Gray, J. S., Wu, R. S., and Or, Y. Y. (2002). Effects of hypoxia and organic enrichment on the coastal marine environment. Marine Ecology Progress Series, 238, 249–279. http://doi.org/10.3354/meps238249
Grego, M., De Troch, M., Forte, J., and Malej, A. (2009). Main meiofauna taxa as an indicator for assessing the spatial and seasonal impact of fish farming. Marine Pollution Bulletin, 58(8), 1178–1186. http://doi.org/10.1016/j.marpolbul.2009.03.020
Guilini, K., Bezerra, T. N., Eisendle-Flöckner, U., Deprez, T., Fonseca, G., Holovachov, O., … Vincx, M. (2017). NeMys: World Database of Free-Living Marine Nematodes.
Guilini, K., Soltwedel, T., van Oevelen, D., and Vanreusel, A. (2011). Deep-sea nematodes actively colonise sediments, irrespective of the presence of a pulse of organic matter: Results from an in-situ experiment. PLoS ONE, 6(4). http://doi.org/10.1371/journal.pone.0018912
Gutzmann, E., Martínez Arbizu, P., Rose, A., and Veit-Köhler, G. (2004). Meiofauna communities along an abyssal depth gradient in the Drake Passage. Deep-Sea Research Part II: Topical Studies in Oceanography, 51(14–16), 1617–1628. http://doi.org/10.1016/j.dsr2.2004.06.026
Heip, C. H. R., Herman, P. M. J., and Soetaert, K. (1998). Indices of diversity and evenness. Oceanis, 24(4), 61–88.
Heip, C. H. R., Vincx, M., and Vrank, G. (1985). The ecology of marine nematodes. Oceanography and Marine Biology - An Annual Review.
Higgins, R. P., and Thiel, H. (1988). Introduction to the study of meiofauna. Smithsonian Institution Press, Washington, DC.
Hill, M. O. (1973). Diversity and evenness: a unifying notation and its consequences 1. Ecology, 54(2), 427–432.
Holmer, M., Duarte, C. M., Heilskov, A., Olesen, B., and Terrados, J. (2003). Biogeochemical conditions in sediments enriched by organic matter from net-pen fish farms in the Bolinao area, Philippines. Marine Pollution Bulletin, 46(11), 1470–1479. http://doi.org/10.1016/S0025-326X(03)00281-9
Holmer, M., Marba, N., Diaz-Almela, E., Duarte, C. M., Tsapakis, M., and Danovaro, R. (2007). Sedimentation of organic matter from fish farms in oligotrophic Mediterranean assessed through bulk and stable isotope (δ13C and δ15N) analyses. Aquaculture, 262(2–4), 268–280. http://doi.org/10.1016/j.aquaculture.2006.09.033
Hurlbert, S. H. (1971). The nonconcept of species diversity: a critique and alternative parameters. Ecology, 52(4), 577–586.
Josefson, A. B., and Widbom, B. (1985). Differential response of benthic macrofauna and meiofauna to hypoxia in the Gullmar Fjord basin. Marine Biology, 100, 31–40.
Kutti, T., Ervik, A., and Høisaeter, T. (2008). Effects of organic effluents from a salmon farm on a fjord system. III. Linking deposition rates of organic matter and benthic productivity. Aquaculture, 282(1–4), 47–53. http://doi.org/10.1016/j.aquaculture.2008.06.032
Kutti, T., Hansen, P. K., Ervik, A., Høisaeter, T., and Johannessen, P. (2007). Effects of organic effluents from a salmon farm on a fjord system. II. Temporal and spatial patterns in infauna community composition. Aquaculture, 262(2–4), 355–366. http://doi.org/10.1016/j.aquaculture.2006.10.008
22
Lambshead, P. J. D. (1986). Sub-catastrophic sewage and industrial waste contamination as revealed by marine nematode faunal analysis. Marine Ecology Progress Series, 29(29), 247–260. http://doi.org/10.3354/meps029247
Lebrato, M., Mendes, P. D. J., Steinberg, D. K., Cartes, J. E., Jones, B. M., Birsa, L. M., … Oschlies, A. (2013). Jelly biomass sinking speed reveals a fast carbon export mechanism. Limnology and Oceanography, 58(3), 1113–1122. http://doi.org/10.4319/lo.2013.58.3.1113
Lebrato, M., Pitt, K. A., Sweetman, A. K., Jones, D. O. B., Cartes, J. E., Oschlies, A., … Billett, D. S. M. (2012). Jelly-falls historic and recent observations: A review to drive future research directions. Hydrobiologia, 690(1), 227–245. http://doi.org/10.1007/s10750-012-1046-8
Mahaut, M. L., Sibuet, M., and Shirayama, Y. (1995). Weight-dependent respiration rates in deep-sea organisms. Deep-Sea Research Part I, 42(9), 1575–1582. http://doi.org/10.1016/0967-0637(95)00070-M
Marques, J. C., Salas, F., Patricio, J., Teixeira, H., and Neto, J. M. (2010). Ecological Indicators for Coastal and Estuarine Environmental Assessment: A User Guide. International Journal of the Society for Underwater Technology, 29(1), 59–59. http://doi.org/10.3723/ut.29.059
Mazzola, A. (2000). Fish-farming effects on benthic community structure in coastal sediments: analysis of meiofaunal recovery. ICES Journal of Marine Science, 57(5), 1454–1461. http://doi.org/10.1006/jmsc.2000.0904
Mevenkamp, L., Stratmann, T., Guilini, K., Moodley, L., van Oevelen, D., Vanreusel, A., … Sweetman, A. K. (2017). Impaired Short-Term Functioning of a Benthic Community from a Deep Norwegian Fjord Following Deposition of Mine Tailings and Sediments. Frontiers in Marine Science, 4(May), 1–16. http://doi.org/10.3389/fmars.2017.00169
Mirto, S., Bianchelli, S., Gambi, C., Krzelj, M., Pusceddu, A., Scopa, M., … Danovaro, R. (2010). Fish-farm impact on metazoan meiofauna in the Mediterranean Sea: Analysis of regional vs. habitat effects. Marine Environmental Research, 69(1), 38–47. http://doi.org/10.1016/j.marenvres.2009.07.005
Mirto, S., Gristina, M., Sinopoli, M., Maricchiolo, G., Genovese, L., Vizzini, S., and Mazzola, A. (2012). Meiofauna as an indicator for assessing the impact of fish farming at an exposed marine site. Ecological Indicators, 18, 468–476. http://doi.org/10.1016/j.ecolind.2011.12.015
Mirto, S., La Rosa, T., Gambi, C., Danovaro, R., and Mazzola, A. (2002). Nematode community response to fish-farm impact in the western Mediterranean. Environmental Pollution, 116(2), 203–214. http://doi.org/10.1016/S0269-7491(01)00140-3
Modig, H., and Ólafsson, E. (1998). Responses of Baltic benthic invertebrates to hypoxic events. Journal of Experimental Marine Biology and Ecology, 229(1), 133–148. http://doi.org/10.1016/S0022-0981(98)00043-4
Moreno, M., Vezzulli, L., Marin, V., Laconi, P., Albertelli, G., and Fabiano, M. (2008). The use of meiofauna diversity as an indicator of pollution in harbours. ICES Journal of Marine Science, 65(8), 1428–1435. http://doi.org/10.1093/icesjms/fsn116
Neofitou, N., Vafidis, D., and Klaoudatos, S. (2010). Spatial and temporal effects of fish farming on benthic community structure in a semi-enclosed gulf of the Eastern Mediterranean. Aquaculture Environment Interactions, 1(2), 95–105. http://doi.org/Doi 10.3354/Aei00010
Pape, E., van Oevelen, D., Moodley, L., Soetaert, K., and Vanreusel, A. (2013). Nematode feeding strategies and the fate of dissolved organic matter carbon in different deep-sea sedimentary environments. Deep-Sea Research Part I, 80(2013), 94–110.
R Core Team. (2013). A language and environment for statistical computing. R Foundation for Statistical Computing, Vienna, Austria.
Ramsing, N., and Gundersen, J. (2011). Seawater and gases. Tabulated physical parameters of interest to people working with microsensors in marine systems. Www.Unisense.Com, 20.
Riemann, L., Titelman, J., and Båmstedt, U. (2006). Links between jellyfish and microbes in a jellyfish dominated fjord. Marine Ecology Progress Series, 325(2003), 29–42.
RStudio Team. (2015). RStudio: Integrated Development for R. Retrieved from http://www.rstudio.com
Seinhorst, J. W. (1959). A rapid method for the transfer of nematodes from fixative to anhydrous glycerin. Nematologica, 4(1), 67–69.
Skogen, M. D., Eknes, M., Asplin, L. C., and Sandvik, A. D. (2009). Modelling the environmental effects of fish farming in a Norwegian fjord. Aquaculture, 298(1–2), 70–75. http://doi.org/10.1016/j.aquaculture.2009.10.018
23
Smith, R. W., Bianchi, T. S., Allison, M., Savage, C., and Galy, V. (2015). High rates of organic carbon burial in fjord sediments globally. Nature Geoscience, 8(May), 450–453. http://doi.org/10.1038/ngeo2421
Soetaert, K., Franco, M. A., Lampadariou, N., Muthumbi, A., Steyaert, M., Vandepitte, L., … Vanaverbeke, J. (2009). Factors affecting nematode biomass, length and width from the shelf to the deep sea. Marine Ecology Progress Series, 392(1975), 123–132. http://doi.org/10.3354/meps08202
Soetaert, K., and Heip, C. H. R. (1990). Sample-size dependence of diversity indices and the determination of sufficient sample size in a high-diversity deep-sea environment. Marine Ecology Progress Series, 305–307.
Sørnes, T. A., Aksnes, D. L., Båmstedt, U., and Youngbluth, M. J. (2007). Causes for mass occurrences of the jellyfish Periphylla periphylla: A hypothesis that involves optically conditioned retention. Journal of Plankton Research, 29(2), 157–167. http://doi.org/10.1093/plankt/fbm003
Soto, L. A., Salcedo, D. L., Arvizu, K., and Botello, A. V. (2017). Interannual patterns of the large free-living nematode assemblages in the Mexican Exclusive Economic Zone, NW Gulf of Mexico after the Deepwater Horizon oil spill. Ecological Indicators, 79(May), 371–381. http://doi.org/10.1016/j.ecolind.2017.03.058
Sweetman, A. K., and Chapman, A. (2011). First observations of jelly-falls at the seafloor in a deep-sea fjord. Deep-Sea Research Part I: Oceanographic Research Papers, 58(12), 1206–1211. http://doi.org/10.1016/j.dsr.2011.08.006
Sweetman, A. K., and Chapman, A. (2015). First assessment of flux rates of jellyfish carcasses (jelly-falls) to the benthos reveals the importance of gelatinous material for biological C-cycling in jellyfish-dominated ecosystems. Frontiers in Marine Science, 2(July), 1–7. http://doi.org/10.3389/fmars.2015.00047
Sweetman, A. K., Chelsky, A., Pitt, K. A., Andrade, H., van Oevelen, D., and Renaud, P. E. (2016). Jellyfish decomposition at the seafloor rapidly alters biogeochemical cycling and carbon flow through benthic food-webs. Limnology and Oceanography, 61(4), 1449–1461. http://doi.org/10.1002/lno.10310
Sweetman, A. K., Norling, K., Gunderstad, C., Haugland, B. T., and Dale, T. (2014). Benthic ecosystem functioning beneath fish farms in different hydrodynamic environments. Limnology and Oceanography, 59(4), 1139–1151. http://doi.org/10.4319/lo.2014.59.4.1139
Titelman, J., Riemann, L., Srnes, T. A., Nilsen, T., Griekspoor, P., and Båmstedt, U. (2006). Turnover of dead jellyfish : stimulation and retardation of microbial activity. Marine Ecology Progress Series, 325, 43–58.
Valdemarsen, T., Bannister, R. J., Hansen, P. K., Holmer, M., and Ervik, A. (2012). Biogeochemical malfunctioning in sediments beneath a deep-water fish farm. Environmental Pollution, 170, 15–25. http://doi.org/10.1016/j.envpol.2012.06.007
van Oevelen, D., Soetaert, K., Middelburg, J. J., Herman, P. M. J., Moodley, L., Hamels, I., … Heip, C. H. R. (2006). Carbon flows through a benthic food web: Integrating biomass, isotope and tracer data. Journal of Marine Research, 64(3), 453–482. http://doi.org/10.1357/002224006778189581
Warwick, R. M., Platt, H. M., and Somerfield, P. J. (1998). Free living marine nematodes. Part III: Britisch Monhysterids. Synopsis of the British Fauna. The Linnean Society of London and the Estuarine and Brackish-Water Sciences Association, London, 38.
Weston, D. P. (1990). Quantitative examination of macrobenthic community changes along an organic enrichment gradient. Marine Ecology Progress Series, 61(2), 233–244. http://doi.org/10.3354/meps061233
Wieser, W. (1953). Die Beziehung zwischen Mundhöhlengestalt, Ernährungsweise und Vorkommen bei freilebenden marinen Nematoden.. Arkiv Für Zoologi, 4, 439–484.
Witte, U., Aberle, N., Sand, M., and Wenzhöfer, F. (2003). Rapid response of a deep-sea benthic community to POM enrichment: an in-situ experimental study. Marine Ecology Progress Series, 251, 27–36. http://doi.org/10.3354/meps251027
Woulds, C., Andersson, J. H., Cowie, G. L., Middelburg, J. J., and Levin, L. A. (2009). The short-term fate of organic carbon in marine sediments: Comparing the Pakistan margin to other regions. Deep-Sea Research Part II: Topical Studies in Oceanography, 56(6–7), 393–402. http://doi.org/10.1016/j.dsr2.2008.10.008
Youngbluth, M. J., and Båmstedt, U. (2001). Distribution, abundance, behavior and metabolism of Periphylla periphylla, a mesopelagic coronate medusa in a Norwegian fjord. Hydrobiologia, 451, 321–333.









