Waarom samenleven? Het groepsleven onderzocht bij een graafwesp
Dieren leven vaak in groep: denk maar aan roedels wolven, bijen- en mierenkolonies, scholen vissen, troepen vogels, kuddes bizons… Maar hoe en waarom ontstaan zulke levenswijzen? Bijen en wespen zijn interessante dieren om groepsleven te bestuderen. Zij kunnen ons meer leren over het ontstaan, de voordelen van en de processen betrokken bij het leven in groep. Het begrijpen van deze complexe processen in de natuur helpt ons ook die natuur beter te beschermen.
De vraag waarom dieren (en mensen) in groepen leven, heeft gedragsbiologen en sociologen al lang gefascineerd. Hebben dieren die in groep leven minder kans om ten prooi te vallen aan predatoren of kunnen ze zich beter verdedigen? Of heeft het sociale voordelen, zoals samen gemakkelijker voedsel of leefgebied vinden en delen? Ook bij de mens is nog niet helemaal begrepen hoe onze complexe maatschappij evolutionair tot stand kwam en wat nu precies de belangrijkste voordelen waren en zijn. Een interessante groep in het dierenrijk om dit te onderzoeken zijn de hyper-sociale bijen, wespen en mieren (de Hymenoptera-orde). Ons onderzoek bekeek het groepsleven van een graafwesp, die wel in groep nesten maakt, maar waarbij elk individu de eigen larven opvoedt. Dit vormt tussenstap van een solitaire levenswijze (op z’n eentje) naar een hypersociale structuur, zoals bij honingbijen en mieren, die grote kolonies vormen waarbij elk individu werkt voor de samenleving. Deze tussenstap bestuderen is net interessant om het ontstaan van complexe sociale levensvormen beter te begrijpen.
De harkwesp

De graafwesp die voor dit onderzoek werd bestudeerd is de harkwesp, Bembix rostrata. Deze wesp is niet zoals de wespen die in de zomer in je limonade kruipen en durven steken. De harkwesp is heel onschuldig want steekt geen mensen, heeft golvende gele en zwarte strepen, een meer gedrongen uiterlijk en onmiskenbare mooie, grote groene ogen. Het is een heel zeldzaam beestje dat in duingebieden voorkomt. In België komt dit insect nog maar op drie plaatsen voor: de Westkust, Geel-Bel en Bernissart. De volwassen harkwespen leven van juni tot september. Na bevrucht te zijn door een mannetje, graven vrouwtjes een nest in het zand met de letterlijke harkjes op hun poten: stevige haren op hun voorpoten. Eens ze een nestje gemaakt hebben, beginnen ze vliegen te vangen om hun larve te voeden; zelf drinken ze nectar. Er zit één larve in een nestje, en ze maken in hun leven zo’n 5 à 6 nestjes. Op het einde van de zomer sterven de volwassen harkwespen. De larven onder de grond verpoppen en wachten op de volgende zomer om uit te sluipen en de cyclus helemaal opnieuw te beginnen. Doordat één vrouwtje niet zo veel nakomelingen heeft en ze hun nestjes in het zand maken, zijn de nestplaatsen heel gevoelig voor vertrappeling door mensen en grazers in duingebieden.
De koekoek van de harkwesp
Wanneer de harkwesp naar zijn nest vliegt om zijn larve te bevoorraden met nieuwe prooien, liggen kleine vliegjes met rode ogen op de loer. Zij proberen hun eitjes op de prooi van de harkwesp te leggen. De vliegen-nakomelingen eten het voedsel op dat voor de harkwesplarve was gebracht, net zoals een koekoeksjong dat doet bij zangvogels. De harkwesp probeert natuurlijk deze koekoek-vliegjes te vermijden… Misschien biedt in groep leven bescherming?
Het onderzoek
Dit onderzoek wou achterhalen hoe groepen nesten van de harkwesp ontstaan. Komt dit doordat er maar weinig geschikte nestplaatsen zijn en ze daarom dicht bijeen zitten of kunnen ze zich in groep beter beschermen tegen parasieten?
In de zomer van 2016 werd een populatie harkwespen in het natuurreservaat De Westhoek in detail onderzocht. Vrouwtjes harkwespen kregen een genummerd plaatje op de rug geplakt en werden opgevolgd. Hun nesten werden met vlagjes aangeduid en er werd genoteerd als een koekoekvliegje een nest ‘besmette’. Om de geschiktheid van nestplaatsen in kaart te brengen werden met een drone hoge resolutie luchtfoto’s genomen van het terrein.
De resultaten
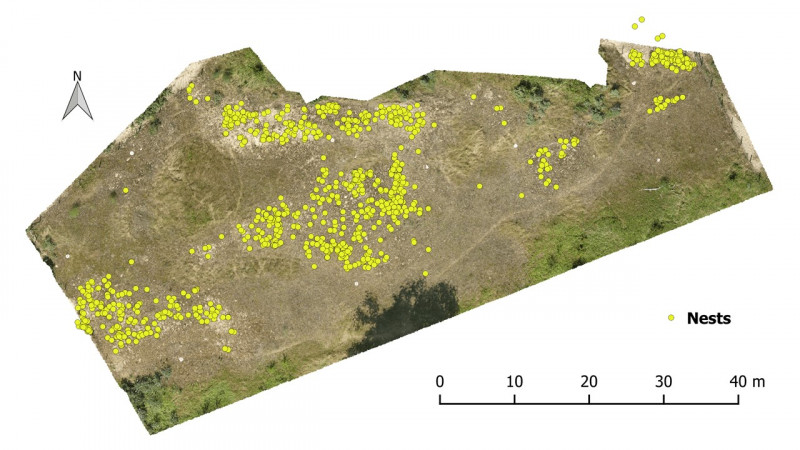
Onze drone-luchtfoto’s toonden dat harkwespen warme plekjes met weinig vegetatie verkiezen. Zulke nestplaatsen, met de juiste voorwaarden, zijn weinig voorhanden: de wespen moeten delen en op een geschikt stuk duin samen nesten maken. Is dat de enige reden om in groep te leven? Nee, er is meer aan de hand. Wij vonden dat een individu die een nestplaats kiest waar veel andere harkwespen hun nesten maken, minder kans hebben om besmet te worden door een koekoek-vliegje. Dit wordt in de biologie beschreven als een ‘selfish-herd mechanisme’ of ‘zelfzuchtige kudde’. Een individuele zebra zal in een grote kudde minder kans hebben gevangen te worden door een leeuw. Ook al trekt een grote groep meer leeuwen aan, het voordeel van een veel grotere groep weegt nog altijd op tegen de extra leeuwen die worden aangetrokken. Ditzelfde mechanisme zorgt ervoor dat de harkwesp plaatsen opzoekt met vele andere soortgenoten en zit wellicht diep geworteld in deze wesp. Hierdoor zullen ze niet vlug nieuwe, geschikte gebieden koloniseren. Dit was al langer gekend bij deze soort, maar dit onderzoek wees de juiste oorzaak aan. Het probleem is dus niet mobiliteit, want de harkwesp is een goede vlieger, maar de beperking van de sociale context: ze willen dat soortgenoten al aanwezig zijn, zodat ze meer beschermd zijn tegen parasieten. Samen met de gevoeligheid voor vertrappeling is dit belangrijke informatie voor het natuurbeheer in de duinen. Het helpt om beter te begrijpen waarom de harkwesp op bepaalde plekken voorkomt en op andere niet, ook al zijn die plekjes in de duinen wel geschikt.
Het nut van deze gedetailleerde studie?
Dit onderzoek is een stukje van de puzzel om het hoe en waarom van het leven in groep beter te begrijpen en hoe dat in de natuur op verschillende manieren is ontstaan en geëvolueerd. Het geeft ons ook inzicht in de dieperliggende processen achter nestplaatskeuze bij de harkwesp, wat ons in staat stelt de verspreiding van de harkwesp beter te begrijpen. Inzicht in complexe mechanismen in de natuur laat ons toe te beseffen dat de natuur niet eenduidig reageert op veranderingen door mens en klimaat. Als we meer doorgronden, kunnen we optimaler beschermen.
Bibliografie
- Allouche, O., Tsoar, A. & Kadmon, R. (2006). Assessing the accuracy of species distribution models: prevalence, kappa and the true skill statistic (TSS). Journal of Applied Ecology, 43, 1223–1232.
- Aplin, L.M., Farine, D.R., Morand-Ferron, J., Cockburn, A., Thornton, A. & Sheldon, B.C. (2015). Experimentally induced innovations lead to persistent culture via conformity in wild birds. Nature, 518, 538–541.
- Baddeley, A. (2010). Analysing spatial point patterns in R. 4th edn. CSIRO. pp. 232.
- Baddeley, A., Rubak, E. & Turner, R. (2015). Spatial Point Patterns: Methodology and Applications with R. London: Chapman and Hall/CRC. pp. 810. http://www.spatstat.org/.
- Bailey, D.W., Gross, J.E., Laca, E.A., Rittenhouse, L.R., Coughenour, M.B., Swift, D.M. & Sims, P.L. (1996). Mechanisms That Result in Large Herbivore Grazing Distribution Patterns. Journal of Range Management, 49, 386–400.
- Banse, K. (2007). Do we live in a largely top-down regulated world? Journal of Biosciences, 32, 791–796.
- Bélisle, M. (2005). Measuring Landscape Connectivity: the Challenge of Behavioural Landscape Ecology. Ecology, 86, 1988–1995.
- Belles-Isles, J.C. & Picman, J. (1986). Nesting Losses and Nest Site Preferences in House Wrens. The Condor, 88, 483–486.
- Bjornstad, O.N. (2016). ncf: Spatial Nonparametric Covariance Functions. https://cran.r-project.org/package=ncf.
- Blonder, B. (2015). timeordered: Time-ordered and time-aggregated network analyses. https://cran.r-project.org/package=timeordered.
- Bonte, D. (2005). Anthropogenic induced changes in nesting densities of the dune-specialised digger wasp Bembix rostrata (Hymenoptera: Sphecidae). Eur. J. Entomol., 102, 809–812.
- Bonte, D., Lens, L., Maelfait, J.P., Hoffmann, M. & Kuijken, E. (2003). Patch quality and connectivity influence spatial dynamics in a dune wolfspider. Oecologia, 135, 227–233.
- Bowlby, J.N. & Roff, J.C. (1986). Trophic Structure in Southern Ontario Streams. Ecology, 67, 1670–1679.
- Brockmann, H.J. & Dawkins, R. (1979). Joint Nesting in a Digger Wasp as an Evolutionarily Stable Preadaptation to Social Life. Behaviour, 71, 203–245.
- Brown, C.D. & Davis, H.T. (2006). Receiver operating characteristics curves and related decision meas-ures: A tutorial. Chemometrics and Intelligent Laboratory Systems, 80, 24–38.
- Burkepile, D.E. & Hay, M.E. (2006). Herbivore vs. nutrient control of marine primary producers: Context-dependent effects. Ecology, 87, 3128–3139.
- Cahn, J.W. & Hilliard, J.E. (1958). Free Energy of a Nonuniform System. 1. Interfacial Free Energy.
- The Journal of Chemical Physics, 28, 258–267.
- Campomizzi, A.J., Butcher, J.A., Farrell, S.L., Snelgrove, A.G., Collier, B.A., Gutzwiller, K.J., Mor-rison, M.L. & Wilkins, R.N. (2008). Conspecific attraction is a missing component in wildlife habitat modeling. Journal of Wildlife Management, 72, 331–336.
- Chaverri, G. (2010). Comparative social network analysis in a leaf-roosting bat. Behavioral Ecology and Sociobiology, 64, 1619–1630.
- Clark, C.W. & Mangel, M. (1984). Foraging and Flocking Strategies: Information in an Uncertain Environment. The American Naturalist, 123, 626–641.
- Cohen, D. (1966). Optimizing reproduction in a randomly varying environment. J. Theoret. Biol., 12, 119–129.
- Couteron, P. & Lejeune, O. (2001). Periodic spotted patterns in semi-arid vegetation explained by a propagation-inhibition model. Journal of Ecology, 89, 616–628.
- Csardi, G. & Nepusz, T. (2006). The igraph software package for complex network research. InterJournal, Complex Sy, pp. 1695. http://igraph.org.
- Csardi, G. & Nepusz, T. (2013). igraph Reference Manual. pp. 550. http://igraph.sourceforge.net/doc/igraph–docs.
- Davies, N.B., Krebs, J.R. & West, A.S. (2012). An Introduction to Behavioural Ecology. 4th edn. Wiley-Blackwell. pp. 520.Dormann, C.F., McPherson, J.M., Araújo, M.B., Bivand, R., Bolliger, J., Carl, G., Davies, R.G., Hirzel, A., Jetz, W., Kissling, W.D., Kühn, I., Ohlemüller, R., Peres-Neto, P.R., Reineking, B., Schröder, B., Schurr, F.M. & Wilson, R. (2007). Methods to account for spatial autocorrelation in the analysis of species distributional data: A review. Ecography, 30, 609–628.
- Dunson, W.A. & Travist, J. (1991). The Role of Abiotic Factors in Community Organization. The American Naturalist, 138, 1067–1091.
- Dyer, L.A. & Letourneau, D. (2003). Top-down and bottom-up diversity cascades in detrital vs. living food webs. Ecology Letters, 6, 60–68.
- Eggers, S., Griesser, M., Nystrand, M. & Ekman, J. (2006). Predation risk induces changes in nest-site selection and clutch size in the Siberian jay. Proceedings of the Royal Society B, 273, 701–706.
- ESRI (2011a). ArcGIS Desktop: Release 10. ArcMap Tools, Solar Radiation toolset. Environmental Systems Research Institute.
- ESRI (2011b). ArcGIS Desktop: Release 10. Environmental Systems Research Institute. Redlands, CA, USA.
- Ettema, C.H. & Wardle, D.A. (2002). Spatial soil ecology. Trends in Ecology and Evolution, 17, 177–183.
- Evans, H.E. & O’Neill, K.M. (2007). The Sand Wasps: Natural History and Behavior. Harvard University Press, Cambridge, Massachusetts, USA. pp. 340.
- Farine, D.R. & Whitehead, H. (2015). Constructing, conducting and interpreting animal social network analysis. Journal of Animal Ecology, 84, 1144–1163.
- Fewell, J.H. (2003). Social insect networks. Science, 301, 1867–1870.
- Field, J. (2005). The evolution of progressive provisioning. Behavioral Ecology, 16, 770–778.
- Fielding, A.H. & Bell, J.F. (1997). A review of methods for the assessment of prediction errors in conservation presence/absence models. Environmental Conservation, 24, 38–49.
- Forstmeier, W. & Weiss, I. (2004). Adaptive plasticity in nest-site selection in response to changing predation risk. Oikos, 104, 487–499.
- Frankie, G.W., B, V.S., Newstrom, L.E. & Barthell, J.F. (1988). Nest Site and Habitat Preferences of Centris Bees in the Costa Rican Dry Forest. Biotropica, 20, 301–310.
- Fronhofer, E.A., Kubisch, A., Hilker, F.M., Hovestadt, T. & Poethke, H.J. (2012). Why are metapopu-lations so rare? Ecology, 93, 1967–1978.
- Giroux, M.A., Trottier-paquet, M., Bêty, J., Lamarre, V. & Lecomte, N. (2016). Is it safe to nest near bold neighbours? Spatial patterns in predation risk associated with the density of American Golden-Plover nest. PeerJ, 4, 1–13.
- Godfrey, S.S., Moore, J.A., Nelson, N.J. & Bull, C.M. (2010). Social network structure and parasite infection patterns in a territorial reptile, the tuatara (Sphenodon punctatus). International Journal for Parasitology, 40, 1575–1585.
- Gripenberg, S. & Roslin, T. (2007). Up or down in Space? Uniting the Bottom-up versus Top-down Paradigm and Spatial Ecology. Oikos, 116, 181–188.
- Hahn, B.A. & Silverman, E.D. (2006). Social cues facilitate habitat selection: American redstarts establish breeding territories in response to song. Biology letters, 2, 337–40.
- Hairston, N.G., Smith, F.E. & Slobodkin, L.B. (1960). Community Structure, Population and Competi-tion Control. The American Naturalist, XCIV, 421–425.
- Hamilton, W.D. (1971). Geometry for the selfish herd. Journal of Theoretical Biology, 31, 295–311.
- Hammond, J.I., Luttbeg, B. & Sih, A. (2007). Predator and prey space use: Dragonflies and tadpoles in an interactive game. Ecology, 88, 1525–1535.
- Hanski, I., Pakkala, T., Kuussaari, M. & Lei, G. (1995). Metapopulation Persistence of an Endangered Butterfly in a Fragmented Landscape. Oikos, 72, 21–28.
- Hodgson, J.A., Thomas, C.D., Wintle, B.A. & Moilanen, A. (2009). Climate change, connectivity and conservation decision making: Back to basics. J. Appl. Ecol., 46, 964–969.
- Horswill, C., Ratcliffe, N., Green, J.A., Phillips, R.A., Trathan, P.N. & Matthiopoulos, J. (2016). Un-ravelling the relative roles of top-down and bottom-up forces driving population change in an oceanic predator. Ecology, 97, 1919–1928.Hughes, W.O.H., Oldroyd, B.P., Beekman, M. & Ratnieks, F.L.W. (2008). Ancestral Monogamy Shows Kin Selection is Key to the Evolution of Eusociality. Science, 320, 1213–1216.
- Hunter, M.D. & Price, P.W. (1992). Playing Chutes and Ladders: Heterogeneity and the Relative Roles of Bottom-Up and Top- Down Forces in Natural Communities. Ecology, 73, 724–732.
- Hunter, M.D., Varley, G.C. & Gradwell, G.R. (1997). Estimating the relative roles of top-down and bottom-up forces on insect herbivore populations: a classic study revisited. Proceedings of the National Academy of Sciences of the United States of America, 94, 9176–81.
- Hutchinson, G.E. (1957). Concluding remarks. Cold Spring Harbor Symposia on Quantitative Biology, 22, 415–427.
- Inglis, I.R., Langton, S., Forkman, B. & Lazarus, J. (2001). An information primacy model of exploratory and foraging behaviour. Animal Behaviour, 62, 543–557.
- Ji, R., Stegert, C. & Davis, C.S. (2013). Sensitivity of copepod populations to bottom-up and top-down forcing: A modeling study in the Gulf of Maine region. Journal of Plankton Research, 35, 66–79.
- Johnson, M.D. (2007). Measuring Habitat Quality: a Review. The Condor, 109, 489–504.
- Karr, J.R., Dionne, M. & Schlosser, I.J. (1992). Bottom-up versus top-down regulation of vertebrate populations: lessons from birds and fish. In: Effects of resource distribution on animal-plant interactions (eds. Hunter, M.D., Ohgushi, T. & Price, P.W.). Academic Press, San Diego, California, USA, pp. 243–286.
- Kells, A.R. & Goulson, D. (2003). Preferred nesting sites of bumblebee queens (Hymenoptera: Apidae) in agroecosystems in the UK. Biological Conservation, 109, 165–174.
- Kerth, G., Ebert, C. & Schmidtke, C. (2006). Group decision making in fission-fusion societies: evidence from two-field experiments in Bechstein’s bats. Proceedings of the Royal Society B, 273, 2785–90.
- Klein, W.F. & Lefeber, V. (2004). Crabronidae graafwespen. In: De wespen en mieren van Nederland (eds. Peeters, T. & Al., E.). Naturalis en KNNV, pp. 356–430.
- Koh, L.P. & Wich, S.A. (2012). Dawn of drone ecology: low-cost autonomous aerial vehicles for conser-vation. Tropical Conservation Science, 5, 121–132.
- van de Koppel, J. & Crain, C.M. (2006). Scale-dependent inhibition drives regular tussock spacing in a freshwater marsh. The American Naturalist, 168, E136–E147.
- van de Koppel, J., Gascoigne, J.C., Theraulaz, G., Rietkerk, M., Mooij, W.M. & Herman, P.M.J. (2008). Experimental evidence for spatial self-organization and its emergent effects in mussel bed ecosystems. Science, 322, 739–42.
- Krause, J., Lusseau, D. & James, R. (2009). Animal social networks: An introduction. Behavioral Ecology and Sociobiology, 63, 967–973.
- Kristan, W.B. (2003). The role of habitat selection behavior in population dynamics: source-sink systems and ecological traps. Oikos, 103, 457–468.
- Larsen, D.R. (2014). Mark and Recapture Methods: Jolly-Seber Method. Natural Resources Biometrics. Retrieved 15-11-2016 at http://oak.snr.missouri.edu/nr3110/topics/jolly.php.
- Larsson, F. (1986). Increased Nest Density of the Digger Wasp Bembix rostrata as a Response to Parasites and Predators. Entomol. Gener., 12, 71–75.
- Larsson, F. & Tengö, J. (1989). It Is Not Always Good to Be Large; Some Female Fitness Components in a Temperate Digger Wasp, Bembix rostrata (Hymenoptera: Sphecidae). Journal of the Kansas Entomological Society, 62, 490–495.
- Lin, N. & Michener, C.D. (1972). Evolution of Sociality in Insects. The Quarterly Review of Biology, 47, 131–159.
- Liu, Q.X., Doelman, A., Rottschafer, V., de Jager, M., Herman, P.M., Rietkerk, M. & van de Koppel, J. (2013). Phase separation explains a new class of self-organized spatial patterns in ecological systems. Proceedings of the National Academy of Sciences of the United States of America, 110, 11905–11910.
- Liu, Q.X., Rietkerk, M., Herman, P.M.J., Piersma, T., Fryxell, J.M. & van de Koppel, J. (2016). Phase separation driven by density-dependent movement: A novel mechanism for ecological patterns. Physics of Life Reviews, 19, 107–121.
- Livingston, G., Fukumori, K., Provete, D.B., Kawachi, M., Takamura, N. & Leibold, M.A. (2017). Predators regulate prey species sorting and spatial distribution in microbial landscapes. Journal of Animal Ecology, 86, 501–510.
- Lloyd, J.D. & Martin, T.E. (2004). Nest-site preference and maternal effects on offspring growth. Beha-vioral Ecology, 15, 816–823.
- Lobo, J.M., Jiménez-valverde, A. & Real, R. (2008). AUC: A misleading measure of the performance of predictive distribution models. Global Ecology and Biogeography, 17, 145–151.
- Lõhmus, A. (2003). Do Ural owls (Strix uralensis) suffer from the lack of nest sites in managed forests? Biological Conservation, 110, 1–9.
- Maes, D. & Bonte, D. (2006). Using distribution patterns of five threatened invertebrates in a highly fragmented dune landscape to develop a multispecies conservation approach. Biol. Conserv., 133, 490–499.
- Mahon, C.L., Martin, K. & Steventon, J. (2007). Habitat attributes and chestnut-backed chickadee nest site selection in uncut and partial-cut forests. Canadian Journal of Forest Research, 37, 1272–1285.
- Manel, S., Williams, H.C. & Ormerod, S.J. (2001). Evaluating presence absence models in ecology; the need to count for prevalence. Journal of Appied ecology, 38, 921–931.
- Martínez, J.A., Serrano, D. & Zuberogoitia, I. (2003). Predictive models of habitat preferences for the Eurasian eagle owl Bubo bubo: a multiscale approach. Ecography, 26, 21–28.
- Marvin, D.C., Koh, L.P., Lynam, A.J., Wich, S., Davies, A.B., Krishnamurthy, R., Stokes, E., Starkey, R. & Asner, G.P. (2016). Integrating technologies for scalable ecology and conservation. Global Ecology and Conservation, 7, 262–275.
- Matthiopoulos, J., Fieberg, J., Aarts, G., Beyer, H.L., Morales, J.M. & Haydon, D.T. (2015). Establish-ing the link between habitat-selection and animal population dynamics. Ecological Monographs, 85, 150119094816002.
- Mazerolle, M.J. & Villard, M.A. (1999). Patch characteristics and landscape context as predictors of species presence and abundance: A review. Écoscience, 6, 117–124.
- Meserve, P.L., Kelt, D.A., Milstead, W.B. & Gutiérrez, J.R. (2003). Thirteen Years of Shifting Top-Down and Bottom-Up Control. BioScience, 53, 633–646.
- Mistr, S. & Bercovici, D. (2003). A theoretical model of pattern formation in coral reefs. Ecosystems, 6, 61–74.
- Mittelbach, G.G., Osenberg, C.W. & Leibold, M.A. (1988). Trophic Relations and Ontogenetic Niche Shifts in Aquatic Ecosystems. In: Size-Structured Populations (eds. Ebenman, B. & Persson, L.). Springer, Berlin, Heidelberg, pp. 219–235.
- Moskat, C. & Honza, M. (2000). Effect of nest and nest site characteristics on the risk of cuckoo Cuculus canorus parasitism in the great reed warbler Acrocephalus arundinaceus. Ecography, 23, 335–341.
- Muller, K.L., Stamps, J.A., Krishnan, V.V. & Willits, N.H. (1997). The Effects of Conspecific Attraction and Habitat Quality on Habitat Selection in Territorial Birds (Troglodytes aedon). The American Naturalist, 150, 650–661.
- Naug, D. (2008). Structure of the social network and its influence on transmission dynamics in a honeybee colony. Behavioral Ecology and Sociobiology, 62, 1719–1725.
- Naug, D. (2009). Structure and resilience of the social network in an insect colony as a function of colony size. Behavioral Ecology and Sociobiology, 63, 1023–1028.
- Nielsen, E. (1945). Moeurs des Bembex. 7th edn. Spoolia Zool Mus Haun, København. pp. 174.
- Ognyanova, K. (2016). Network Analysis and Visualisation with R and igraph. Tech. rep., NetSciX 2016 School of Code Workshop, Wroclaw, Poland. pp. 64.
- Orrock, J.L., Grabowski, J.H., Pantel, J.H., Peacor, S.D., Barbara, L., Sih, A. & Werner, E.E. (2008). Consumptive and Nonconsumptive Effects of Predators on Metacommunities of Competing Prey. Eco-logy, 89, 2426–2435.
- Peeters, T. (2008). De harkwesp Bembix rostrata - een literatuurstudie. Nieuwsbrief NEV, pp. 40–44.
- Perrin, N. & Mazalov, V. (2000). Local Competition, Inbreeding, and the Evolution of Sex-Biased Dispersal. Am. Nat., 155, 116–127.
- Polidori, C., Casiraghi, M., Di Lorenzo, M., Valarani, B. & Andrietti, F. (2006). Philopatry, nest choice, and aggregation temporal-spatial change in the digger wasp Cerceris arenaria (Hymenoptera: Crabronidae). Journal of Ethology, 24, 155–163.
- Poulin, R. (2010). Network analysis shining light on parasite ecology and diversity. Trends in Parasitology, 26, 492–498.
- Power, M.E. (1992). Top-Down and Bottom-Up Forces in Food Webs: Do Plants Have Primacy? Ecology, 73, 733–746.
- Provoost, S., Ampe, C., Bonte, D., Cosyns, E. & Hoffmann, M. (2004). Ecology, management and monitoring of grey dunes in Flanders. J. Coast. Conserv., 10, 33–42.
- Python Software Foundation (2001). Python Language Reference, version 3.4. http://www.python.org.
- QGIS Development Team (2009). QGIS Geographic Information System. Open Source Geospatial Found-ation. http://qgis.osgeo.org.
- R Core Team (2016). R: A Language and Environment for Statistical Computing. R Foundation for Statistical Computing. https://www.r-project.org/.
- Reinhart, K.O., Packer, A., Van Der Putten, W.H. & Clay, K. (2003). Plant-soil biota interactions and spatial distribution of black cherry in its native and invasive ranges. Ecology Letters, 6, 1046–1050.
- Rietkerk, M., Dekker, S.C., de Ruiter, P.C. & van de Koppel, J. (2004). Self-organized patchiness and catastrophic shifts in ecosystems. Science, 305, 1926–1929.
- Rietkerk, M. & van de Koppel, J. (2008). Regular pattern formation in real ecosystems. Trends in Ecology and Evolution, 23, 169–175.
- Robertson, B.A. & Hutto, R.L. (2006). A framework for understanding ecological traps and an evaluation of existing evidence. Ecology, 87, 1075–1085.
- Sánchez-Zapata, J.A. & Calvo, J.F. (1999). Raptor distribution in relation to landscape composition in semi-arid Mediterranean habitats. Journal of Applied Ecology, 36, 254–262.
- Schöne, H. & Tengö, J. (1981). Competition of Males, Courtship Behaviour and Chemical Communication in the Digger Wasp Bembix rostrata. Behaviour, 77, 44–66.
- Schöne, H. & Tengö, J. (1991). Homing in the Digger Wasp Bembix rostrata - Release Direction and Weather Conditions. Ethology, 87, 160–164.
- Seeley, T.D. & Morse, R.A. (1978). Nest site selection by the honey bee, Apis Mellifera. Insectes Sociaux, 25, 323–337.
- Seitz, R., Lipcius, R. & Hines, A. (2017). Consumer versus resource control and the importance of habitat heterogeneity for marine bivalves. Oikos, 126, 121–135.
- Sih, A. (2013). Understanding variation in behavioural responses to human-induced rapid environmental change: A conceptual overview. Animal Behaviour, 85, 1077–1088.
- Sih, A., Hanser, S.F. & McHugh, K.A. (2009). Social network theory: new insights and issues for behavioral ecologists. Behavioral Ecology and Sociobiology, 63, 975–988.
- Sing, T., Sander, O., Beerenwinkel, N. & Lengnauer, T. (2005). ROCR: visualizing classifier performance in R. Bioinformatics, 21, 7881.
- Slagsvold, T. (1987). Nest Site Preference and Clutch Size in the Pied Flycatcher Ficedula hypoleuca. Ornis Scandinavica (Scandinavian Journal of Ornithology), 13, 165–175.
- Solé, R.V. & Bascompte, J. (2006). Complexity in Ecological Systems. Princeton University Press. pp. 284.
- Stephens, P.A., Sutherland, W.J. & Freckleton, R.P. (1999). What Is the Allee Effect? Oikos, 87, 185–190.
- Storch, I. (1991). Habitat Fragmentation, Nest Site Selection, and Nest Predation Risk in Capercaillie. Ornis Scandinavica (Scandinavian Journal of Ornithology), 22, 213–217.
- Sumpter, D.J.T. (2006). The principles of collective animal behaviour. Philos. Trans. R. Soc. B, 361, 5–22.
- Suryan, R.M., Irons, D.B., Brown, E.D., Jodice, P.G.R. & Roby, D.D. (2006). Site-specific effects on productivity of an upper trophic-level marine predator: Bottom-up, top-down, and mismatch effects on reproduction in a colonial seabird. Progress in Oceanography, 68, 303–328.
- Svensson, B., Lagerlöf, J. & G. Svensson, B. (2000). Habitat preferences of nest-seeking bumble bees (Hymenoptera: Apidae) in an agricultural landscape. Agriculture, Ecosystems & Environment, 77, 247–255.
- van Swaay, C. & Plate, C. (2009). Grootste klappen in de soortenrijke duinen. Vlinders (meetnet vlinders), pp. 14–15.
- Tengö, J., Schöne, H., Kühme, W., Schöne, H. & Kühme, L. (1996). Nesting cycle and homing in the digger wasp Bembix rostrata. Ethol. Ecol. Evol., 8, 207–211.
- Theraulaz, G., Bonabeau, E., Nicolis, S.C., Solé, R.V., Fourcassié, V., Blanco, S., Fournier, R., Joly, J.L., Fernández, P., Grimal, A., Dalle, P. & Deneubourg, J.L. (2002). Spatial patterns in ant colonies. PNAS, 99, 9645–9649.
- Thomas, C.D. (2011a). Anthropocene Park? No alternative. Trends in Ecology and Evolution, 26, 497–498.
- Thomas, C.D. (2011b). Translocation of species, climate change, and the end of trying to recreate past ecological communities. Trends in Ecology and Evolution, 26, 216–221.
- Tinbergen, N. (1951). The Study of Instinct. Oxford Clarendon Press.
- Turing, A.M. (1953). The Chemical Basis of Morphogenesis. Philos. Trans. R. Soc. B, 237, 37–72.
- Van Horne, B. (1983). Density as a Misleading Indicator of Habitat Quality. The Journal of Wildlife Management, 47, 893–901.
- Vanommeslaeghe, A. (2015). Movement patterns, nesting preferences and population estimates of the digger wasp Bembix rostrata. Msc thesis, [MSc thesis]. Unpubl. manuscript, UGent, Depart. Biology.
- Venables, W. & Ripley, B. (2002). Modern Applied Statistics with S. 4th edn. Springer, Yew York. pp. 501.
- Vilà, M. & Hulme, P.E. (2011). Jurassic Park? No thanks. Trends in Ecology and Evolution, 26, 493–494.
- Waarnemingen.be (2016). Harkwesp - Bembix rostrata; 25-06-2016; Wetteren - Speelbos Warandeduinen [OV]; Gertjan Bisschop; waarnemingen.be.
- Walker, M. & Jones, T.H. (2001). Relative roles of top-down and bottom-up forces in terrestrial tritrophic plant-insect herbivore-natural enemy systems. Oikos, 93, 177–187.
- Ward, M.P. & Schlossberg, S. (2004). Conspecific Attraction and the Conservation of Territorial Song-birds. Conservation Biology, 18, 519–525.
- Wcislo, W.T. (1984). Gregarious nesting of a digger wasp as a "selfish herd" response to a parasitic fly (Hymenoptera: Sphecidae; Diptera: Sacrophagidae). Behavioral Ecology and Sociobiology, 15, 157–160.
- Webber, B.L., Scott, J.K. & Didham, R.K. (2011). Translocation or bust! A new acclimatization agenda for the 21st century? Trends in Ecology and Evolution, 26, 493–494.
- Westphal, C., Steffan-Dewenter, I. & Tscharntke, T. (2006). Bumblebees experience landscapes at differ-ent spatial scales: possible implications for coexistence. Oecologia, 149, 289–300.
- White, G.C. & Burnham, K.P. (1999). Program MARK: survival estimation from populations of marked animals. Bird Study, 46, S120–S139.
- Wickham, H. (2009). ggplot2: Elegant Graphics for Data Analysis. Springer-Verlag New York. pp. 213.
- Wuellner, C.T. (1999). Nest site preference and success in a gregarious, ground-nesting bee Dieunomia triangulifera. Ecological Entomology, 24, 471–479.









