Automatische segmentatie van organen in kankertherapie
Machine intelligence is the last invention that humanity will ever need to make.
–
Nick Bostrom.
Geneeskunde is één van de oudste disciplines van de mens. Al in de prehistorie gebruikte men planten en kruiden als natuurlijk medicijn. In de loop der jaren is de mens steeds beter geworden in het voorkomen en genezen van allerlei ziekten en kwalen. Daarnaast werkt men steeds meer interdisciplinair. Zo was het slechts een kwestie van tijd voor men een relatief nieuwe ontwikkeling in de informatica, zijnde het machinaal leren, zou inzetten bij één van de huidige dodelijkste ziekten: kanker.
1 Kanker
We dromen er allemaal van: the cure for cancer. Kijken we naar figuur 1, dan weten we meteen waarom. Kanker is de belangrijkste doodsoorzaak bij mannen en de tweede belangrijkste doodsoorzaak bij vrouwen.
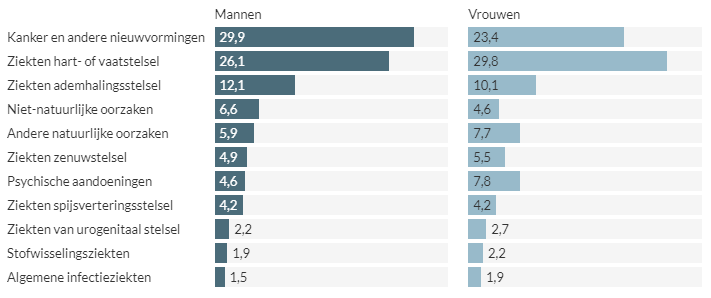
Figuur 1: Relatieve verdeling doodsoorzaken naar geslacht in het Vlaams Gewest in het jaar 2017.
Waarom is dit zo een belangrijke doodsoorzaak? Hier zijn twee grote redenen voor. Allereerst worden we steeds beter in het bestrijden van andere doodsoorzaken. Toen men in 1928 penicilline ontdekte was dit een revolutionair middel in het bestrijden van bacteri"ele infecties. Ook vaccinaties zorgen ervoor dat een hoop ziekten niet meer de onoverwinnelijke vijand zijn die ze vroeger waren. Daarnaast worden we steeds ouder worden en kanker is nu eenmaal een ziekte die meer en meer voorkomt naarmate men ouder wordt.
Dit alles maakt van kanker één van de sterkste vijanden van de mens in zijn eeuwige strijd tegen de dood. Kanker is echter niet één ziekte maar een verzameling van meer dan 100 varianten waardoor een universele oplossing niet voor de hand ligt en er verschillende types behandelingen bestaan. Wij zullen het hebben over één van deze type behandelingen: radiotherapie.
2 Radiotherapie
Concreet gebruikt men bij radiotherapie ioniserende straling om tumoren kapot te stralen. Hierbij wil men uiteraard zo weinig mogelijk gezond weefsel en gezonde organen raken. Dit kan men doen a.d.h.v. twee principes.
Het eerste principe steunt op de stralingsgevoeligheid van tumoren vs. gezond weefsel. Gezonde cellen zijn beter in staat zichzelf te herstellen dan kankercellen. Vooral bij relatief lage stralingsdosissen is dit een sterk verschil. Daarom kiest men er vaak voor de tumor meerdere keren over meerdere dagen te bestralen. Zo wordt de tumor stukje voor stukje kapot bestraald, terwijl het gezonde weefsel tijd heeft gehad om te herstellen tussen twee bestralingen door.
Het tweede principe steunt op het zo goed mogelijk alloceren van de tumor en de gezonde organen. Hiervoor neemt men een 3D-computertomografie (CT) scan van de patiënt die gemakkelijk uit meer dan 250 2-D beelden kan bestaan. Daarna zijn de clinici aan de beurt om zo accuraat mogelijk de organen en de tumor in te tekenen in gespecialiseerde software. Deze software kan dan met die informatie een stralingsplan opstellen met als doel de gezonde organen zoveel mogelijk te sparen en de tumor voldoende te bestralen.
Het intekenen van de organen kan redelijk wat tijd innemen. Ook is deze intekening niet permanent; de patiënt kan wat afgevallen zijn of de tumor kan gekrompen zijn tussen twee bestralingen door. Indien er een methode bestond die de organen automatisch intekende zou men veel sneller kunnen starten aan de behandeling. Daarnaast zou men ook de stralingsplannen kunnen aanpassen tussen twee bestralingen. Daardoor zou de ontvangen dosis verder geoptimaliseerd worden.
3 Machine learning
Hoe leert een baby wandelen? We proberen recht te staan, vallen om en proberen opnieuw. Elke poging leren we wat meer. Hoe houd ik mijn balans? Hoe kan ik de ene voet voor de andere zetten zonder om te vallen? Elke keer leren we van onze vorige actie en worden we beter. Wat als we een machine zouden maken die hetzelfde leerproces heeft? Dan zouden we geen gesofisticeerde algoritmes en diepgaande programma’s moeten schrijven. Slechts een algemene structuur die eender welke taak kan leren door deze taak keer op keer uit te voeren en zichzelf te verbeteren door de gekregen feedback. Dit is de basis van machine learning. We geven het computermodel een doel, definiëren een metriek
dat ons model vertelt hoe goed het de taak kan uitvoeren en zorgen ervoor dat het model zichzelf kan verfijnen aan de
hand van deze feedback.
4 Het onderzoek
Ons doel was om een model te trainen dat automatisch de organen zou intekenen op de CT-beelden. Hiermee wouden we het werk van de clinici verlichten en de variabiliteit tussen clinici onderling weg halen. We gingen ook een stap verder dan vorige onderzoeken. Deze gebruikten vaak technische machine learing metrieken om te oordelen of de intekening al dan niet gelukt was. Wij laadden de gegenereerde oppervlakten in in Raystation (een computerprogramma om het stralingsplan op te maken, zie figuur 2). Hierin werden onze intekeningen vergeleken met de originele intekeningen. Het is namelijk niet die ene technische metriek die zegt hoe goed twee oppervlakten overeenkomen dat praktisch relevant is. Het zijn de klinische gevolgen in de radiotherapie die finaal het meest vertellen of ons model al dan niet toegepast zou kunnen worden.
Onze ingetekende beelden werden positief onthaald door een klinisch expert van het Universitair Ziekenhuis Gent. De expert oordeelde dat de intekeningen van de longen, het hart, de slokdarm, de luchtpijp en het ruggenmerg globaal in orde waren. Kleine systematische fouten leidden soms tot grote verschillen in de technische metrieken, maar bleken klinisch niet relevant.
In de toekomst willen we inzetten op het verder verfijnen door meer data te gebruiken, meer organen te leren herkennen en een 3D-model op te bouwen door de intekening van een CT-beeld niet van enkel dat beeld te laten afhangen, maar ook van de CT-beelden ervoor en erna.
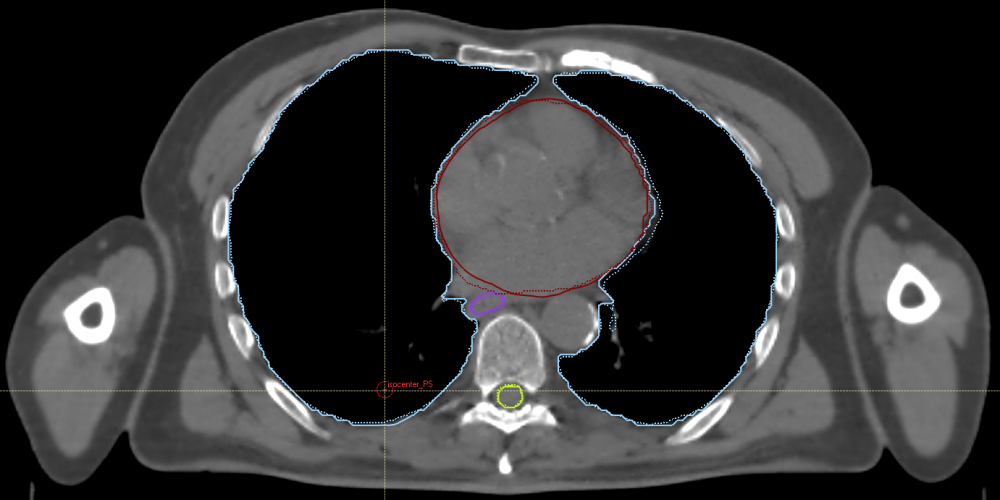
Figuur 2: Voorbeeld van de intekening van één CT-beeld. Rood: hart, lichtblauw: longen, paars: slokdarm, geelgroen: ruggenmerg. Volle lijn: originele intekening, stippellijn: eigen gegenereerde intekening.
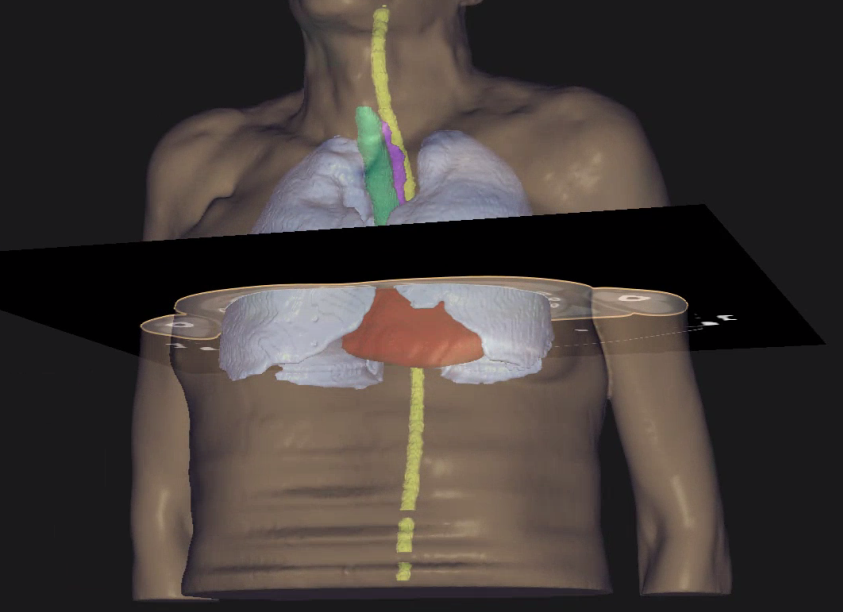
Figuur 3: 3D-beeld van een volledige eigen intekening. De aangeduide doorsnede is het CT-beeld van figuur 2. Rood: hart, lichtblauw: longen, groen: luchtpijp, paars: slokdarm, geelgroen: ruggenmerg.
Bibliografie
1] Statistiekvlaanderen.be. 2020. Doodsoorzaken [online] Geraadpleegd van https://www.statistiekvlaanderen.be/nl/doodsoorzaken.
[2] Salvat, F. and Fern´andez-Varea, J., 2009. Overview of physical interaction models for photon and electron transport used in Monte Carlo codes. Metrologia, 46(2), pp.S112-S138.
[3] Davisson, C. M. (1965). ”Interaction of gamma-radiation with matter”. In Kai Siegbahn (ed.). Alpha-, Beta- and Gamma-ray Spectroscopy: Volume 1. Alpha-. 1. Amsterdam: North-Holland Publishing Company. pp. 37–78.
[4] Ronneberger, O., Fischer, P. and Brox, T., 2020. U-Net: Convolutional Networks For Biomedical Image Segmentation. [online] arXiv.org. Geraadpleegd van https://arxiv.org/abs/1505.04597.
[5] Zhou, X., Takayama, R., Wang, S., Hara, T. and Fujita, H. (2017). Deep learning of the sectional appearances of 3D CT images for anatomical structure segmentation based on an FCN voting method. Medical Physics, 44(10), pp.5221-5233.
[6] Long J, Shelhamer E, Darrell T. Fully convolutional networks for semantic segmentation. Proc CVPR. 2015;3431–3440.
[7] Vesal, S., Ravikumar, N. and Maier, A., 2020. A 2D Dilated Residual U-Net For Multi-Organ Segmentation In Thoracic CT. [online] arXiv.org. Geraadpleegd van https://arxiv.org/abs/1905.07710.
[8] Dong, X., Lei, Y., Wang, T., Thomas, M., Tang, L., Curran, W., Liu, T. and Yang, X., 2020. Automatic Multiorgan Segmentation In Thoraxctimages Using U-Net-GAN.
[9] Tsang, Y., Hoskin, P., Spezi, E., Landau, D., Lester, J., Miles, E. and Conibear, J., 2019. Assessment of contour variability in target volumes and organs at risk in lung cancer radiotherapy. Technical Innovations Patient Support in Radiation Oncology, 10, pp.8-12.
[10] www-pub.iaea.org. 2020. [online] Geraadpleegd van https://wwwpub.iaea.org/MTCD/Publications/PDF/P1679 HH31 web.pdf.
[11] En.wikipedia.org. 2020. Backpropagation. [online] Geraadpleegd van https://en.wikipedia.org/wiki/Backpropagation.
[12] de Vos, B., Wolterink, J., de Jong, P., Viergever, M. and Iˇsgum, I., 2020. 2D Image Classification For 3D Anatomy Localization: Employing Deep Convolutional Neural Networks. https://www.spiedigitallibrary.org/.
[13] Trullo, R., Petitjean, C., Nie, D., Shen, D. and Ruan, S., 2020. Joint Segmentation Of Multiple Thoracic Organs In CT Images With Two Collaborative Deep Architectures. [online] Geraadpleegd van https://www.researchgate.net/publication/319640486.
[14] Vesal, S., Ravikumar, N. and Maier, A., 2020. A 2D Dilated Residual U-Net For Multi-Organ Segmentation In Thoracic CT. [online] arXiv.org. Geraadpleegd van https://arxiv.org/abs/1905.07710.
[15] Tiu, E., 2020. Metrics To Evaluate Your Semantic Segmentation Model. [online] Medium. Geraadpleegd van https://towardsdatascience.com/metrics-to-evaluate-yoursemantic-segment….