Het mysterie van de families waarin inflammatoire darmziekte heerst
Meestal komen patiënten met de ziekte van Crohn of ulceratieve colitis willekeurig voor, maar soms zijn er families met niet één aangetast familielid maar meerdere. In deze families moet er iets meer aan de hand zijn. Zorgt hun genetica ervoor dat ze voorbestemd zijn of hebben ze bepaalde leefgewoontes die het risico verhogen? We weten het niet. Daarom was mijn thesis gefocust op het onderzoeken van de genetica van deze families om te kijken of dit misschien een verklaring geeft.
Personen met zeer veel diarree, dat is wat de meeste mensen weten over de ziekte van Crohn. Deze diarree wordt veroorzaakt door ontsteking in de darmen. Daarom is de ziekte van Crohn één van de twee inflammatoire darmziekten. De andere is ulceratieve colitis. Iets minder gekend, maar daarom niet minder belangrijk. Tegenwoordig worden de twee inflammatoire darmziekten vaak samen onderzocht. Er is alleen een probleem. We weten niet volledig waarom iemand een inflammatoire darmziekte krijgt. Laat staan dat we weten waarom er families zijn met meerdere patiënten.
Na jarenlang onderzoek is er al een tipje van de sluier opgelicht. Inflammatoire darmziekten worden veroorzaakt door zowel genetische als omgevingsfactoren. Omgevingsfactoren zijn bijvoorbeeld dieet en roken. Het slechtste dieet voor inflammatoire darmziekten is het westers dieet met veel vet en suikers. Roken geeft een verhoogde kans op de ziekte van Crohn. Stoppen met roken klinkt als een goede oplossing, maar dat doet dan weer de kans op ulceratieve colitis toenemen. Nooit starten is hier waarschijnlijk het beste. Ik ga het hier verder niet hebben over de invloed van omgevingsfactoren, maar wel over de genetica.
Het genoom is een handleiding voor alles wat in onze cellen gebeurt. Deze handleiding is voor ons geschreven in een codetaal die bestaat uit 4 nucleotiden of bouwblokjes: A, T, G en C. Ons genoom telt ongeveer 9 miljard nucleotiden die elkaar opvolgen in een lange reeks. Alle mensen zijn min of meer hetzelfde en de reeks is daardoor voor iedereen bijna identiek. Bijna, want elke persoon heeft kleine variaties in zijn genoom die onder andere uiterlijk, lengte en vatbaarheid voor ziekten bepalen. De meest voorkomende variaties zijn bepaalde plaatsen waar de ene groep mensen bijvoorbeeld nucleotide A heeft en de rest bijvoorbeeld nucleotide C. Voor veel varianten maakt het niet uit welke je hebt, maar voor sommige geeft één van de twee nucleotiden een risico voor een ziekte. Deze risicovarianten zijn niet allemaal even sterk, sommige hebben een groot effect en andere juist een heel klein. Je kan het vergelijken met een blokkentoren. Er bestaan grote en kleine blokken. Je kan met enkele grote blokken een hoge toren bouwen maar met genoeg kleine bouw je een even hoge toren.
Als je weet welke risicovarianten verbonden zijn met de ziekte en hoe groot hun effect is, kan je voor elke persoon zijn risico berekenen. Een polygene risico score telt alle risicovarianten in het genoom van een persoon op en zorgt ervoor dat risicovarianten met een groter effect zwaarder doorwegen in de score. Hoe hoger je score, hoe groter je risico om de ziekte te ontwikkelen. In de analogie van de blokkentoren, bouwen we de toren met alle blokjes en meten we hoe hoog de toren is. Hoe meer blokjes, hoe hoger je toren. Hoe meer grote blokken, hoe hoger je toren.
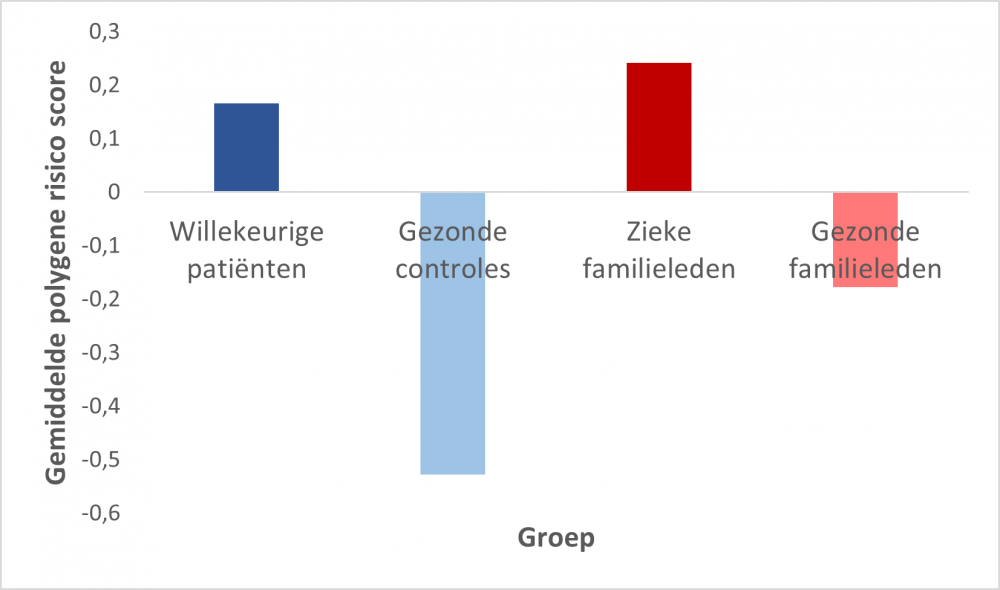
Figuur 1: Gemiddelde polygene risico score per groep
Hoe zit het nu bij de inflammatoire darmziekten? In het begin werd er gezocht naar één gen met een variant met een sterk effect. Ondertussen weten we dat dit niet het geval is. We moeten zoeken naar verschillende varianten met een kleiner effect. Om een inflammatoire darmziekte te ontwikkelen moet je dus voldoende risicovarianten dragen. Jouw blokkentoren moet een bepaalde hoogte bereiken. Zeer grote studies hebben ongeveer 240 regio’s gevonden waar er zich risicovarianten in verschuilen. Deze studies bepalen niet alleen welke varianten risicovarianten zijn, maar ook hoe groot hun effect is. In de vergelijking met onze toren vinden ze uit welke blokjes onze toren is opgebouwd en zelfs hoe groot elk blokje is. Met 240 regio’s kunnen we niet volledig verklaren waarom iemand een inflammatoire darmziekte ontwikkelt, maar ze geven wel voldoende informatie om polygene risico scores te berekenen.
Als de scores goed werken, dan zouden mensen met de ziekte hogere scores hebben dan mensen zonder de ziekte (Figuur 1). Dit is inderdaad zo. Hetzelfde patroon van hogere scores in patiënten zien we ook in families tussen de gezonde en zieke familieleden. Dus ook in families spelen de risicovarianten met een klein effect een belangrijke rol. Bovendien blijken familiale en willekeurige patiënten een gelijkaardige score te hebben. Interessant genoeg geldt dit niet voor gezonde familieleden en niet-verwante controles. De gezonde familieleden hebben een hogere score, en dus meer risicovarianten, dan niet-verwante controles, maar niet zoveel als patiënten. In het algemeen lijkt het dat in deze families er zeer veel risicovarianten circuleren en degene die de ziekte ontwikkelen er net iets meer erven.
De vraag is nu of al deze families inderdaad meer risicovarianten hebben. Hiervoor nam ik de polygene risico scores van alle familieleden van één familie en berekende het gemiddelde (Figuur 2). Als er in de hele familie, zowel de gezonde als zieke familieleden, meer risicovarianten circuleren, dan zou de gemiddelde score zeer hoog moeten zijn. Voor net iets minder dan de helft van de onderzochte families was dit ook het geval. Enkele families daarentegen hadden extreem weinig van deze risicovarianten. Veel risicovarianten met een klein effect kan dus een verklaring zijn voor een deel van de families, maar niet voor allemaal.
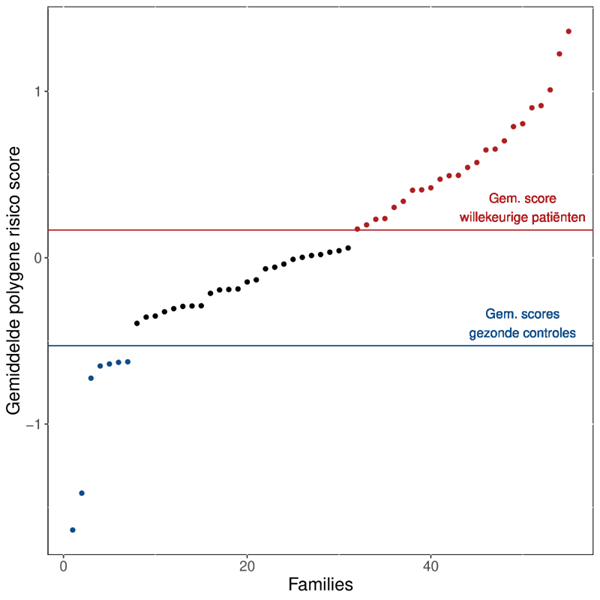
Figuur 2: Familiale polygene risico scores
Hebben we hiermee het mysterie opgelost? Niet echt! De resultaten geven maar een verklaring voor een deel van de families en die is zelfs nog niet volledig. Risico scores geven een samenvatting en geen details. Die zullen nog uitgezocht moeten worden. Voor de andere families is het niet duidelijk waar we het antwoord moeten zoeken. Zeldzame varianten, het dieet of iets volledig anders? Het mysterie is duidelijk nog niet opgelost.









