HET GEBRUIK VAN MUIZEN EN VIRUSSEN IN DE ZOEKTOCHT NAAR EEN MEDICIJN VOOR EPILEPSIE
HET GEBRUIK VAN MUIZEN EN VIRUSSEN IN DE ZOEKTOCHT NAAR EEN MEDICIJN VOOR EPILEPSIE
DE VALLENDE ZIEKTE
De vallende ziekte is vermoedelijk één van de meest mysterieuze ziekte. Volgens de Grieken en de Romeinen stonden mensen met een epileptische aanval in contact met God. Dit staat in sterk contrast met wat de mensen ten tijde van de Middeleeuwen geloofden, namelijk dat ze bezeten waren door de duivel. Ondertussen zijn beide opvattingen uitgesloten en zijn wetenschappers tot de conclusie gekomen dat epilepsie een aandoening van het centraal zenuwstelsel is.
EPILEPSIE: EEN NEUROLOGISCHE AANDOENING
Ongeveer 1% van de bevolking lijdt aan epilepsie. Een epileptische aanval wordt gekenmerkt door veranderingen in het bewustzijn, abnormale gevoelswaarnemingen, automatismen, etc. Het klassieke beeld van stuiptrekkende patiënten komt dus zeker niet bij alle epileptici voor.
Onze hersenen zijn opgebouwd uit verschillende types cellen waaronder neuronen. Neuronen maken een belangrijk onderdeel uit van de hersencellen en zijn in staat om prikkels van de ene cel naar de andere cel door te geven. Er zijn excitatoire neuronen die andere neuronen kunnen activeren en inhibitoire neuronen die andere neuronen kunnen deactiveren. Bij een epileptische aanval is er te veel activiteit van de excitatoire neuronen of te weinig activiteit van de inhibitoire neuronen waardoor er een kortsluiting in de hersenen ontstaat.
Vooraleer men op zoek kan gaan naar een therapie om epileptische aanvallen te reduceren, hebben we nood aan een populatie waar we ons medicijn op kunnen testen. Aangezien het totaal onverantwoord is om een geneesmiddel direct op mensen te testen, gebruiken we proefdieren. In deze studieopzet wordt er gebruik gemaakt van muizen. In de hersenen van de muis injecteert men kainaat, een chemische stof, terwijl de muis verdoofd is. Kainaat induceert eveneens een kortsluiting in de hersenen. Hierdoor vertonen de muizen een gelijkaardig fenotype als epileptici.
Vervolgens worden een aantal elektroden geïmplanteerd in de hersenen. Aan de hand van deze elektroden kunnen we potentiaalverschillen meten en op een objectieve manier de epileptische aanvallen kwantificeren. Het aantal en duur van de epileptische aanvallen zonder medicatie wordt vergeleken met de totale aanvalsduur met medicatie om te zien of er een effect is van de therapie.
HET GEBRUIK VAN EEN VIRUS ALS THERAPIE VOOR EPILEPSIE
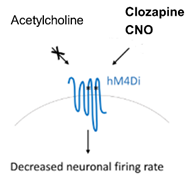
Het eerste luik van de therapie bestaat uit de injectie van een virus in de hersenen. Op het eerste zicht lijkt het nogal controversieel om iemand te besmetten met een virus om de patiënt beter te maken. Na het lezen van dit artikel zal je hopelijk exact verstaan hoe dit mogelijk is. Een virus is in essentie een zeer nuttig organisme: het is in staat om cellen te transfecteren. Wanneer een cel getransfecteerd is, worden naast bepaalde DNA-sequenties van de gastcel eveneens bepaalde DNA-sequenties van het virus afgeschreven. Met behulp van genomic engineering kunnen we de DNA-sequentie van het virus op dergelijke wijze manipuleren zodat de getransfecteerde cel een eiwit naar keuze tot expressie zal brengen. In deze thesis zullen uitsluitend de excitatoire neuronen besmet worden met het virus. Enkel deze cellen zullen de hM4Di-receptor tot expressie brengen. Het voordeel van de gemodificeerde receptor is dat de receptor enkel actief is wanneer een bepaalde molecule, die normaalgezien niet in het lichaam voorkomt, aanwezig is. Dit stelt ons met andere worden in staat om de receptor te activeren op het moment dat wij ervoor kiezen om deze te activeren.
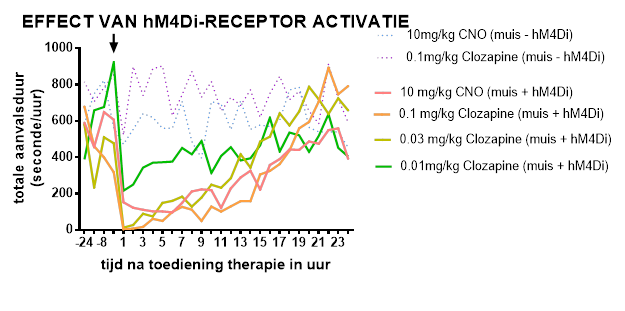
In het tweede luik injecteert men Clozapine-N-Oxide (CNO) of clozapine in de buikholte van de muis. Deze chemische moleculen binden op de hM4Di-receptor die tot expressie komt op de excitatoire neuronen. Activatie van deze DREADD-receptor zorgt ervoor dat de activiteit van deze specifieke groep neuronen afgezwakt wordt. Op deze manier kan het onevenwicht in activiteit van excitatoire en inhibitoire neuronen hersteld worden. De resultaten afkomstig uit de thesis lijken alvast deze hypothese te bevestigen: de totale aanvalsduur is significant lager wanneer de muizen behandeld zijn met de therapie in vergelijking met de baseline.
IS ER INVLOED VAN DE THERAPIE OP HET GEDRAG VAN MUIZEN?
Activiteit van bepaalde hersencellen blokkeren, heeft dat geen invloed op het normaal functioneren van de hersenen? Voor zover reeds onderzocht is, is dit gelukkig niet het geval. In deze experimenten heeft men de activiteit van excitatoire neuronen ter hoogte van de hippocampus gedempt. De hippocampus is een structuur in de hersenen die een belangrijke rol speelt in geheugenprocessen, locomotie en angst. Een mogelijkse verstoring van deze functies werden nagegaan met behulp van gedragstesten. Benieuwd hoe je het geheugen van een muis kan testen? Neem dan zeker eens een kijkje in mijn thesis!

Bibliografie
1. Singh A, Trevick S (2016) The Epidemiology of Global Epilepsy. Neurol Clin 34: 837–847. 2. Fisher RS, et al. (2014) ILAE Official Report: A practical clinical definition of epilepsy. Epilepsia 55: 475– 482. 3. Scheffer IE, et al. The Organization of the Epilepsies: Report of the ILAE Commission on Classification and Terminology. 4. Reddy DS, Kuruba R (2013) Experimental models of status epilepticus and neuronal injury for evaluation of therapeutic interventions. Int J Mol Sci 14: 18284–18318. 5. Pitkänen A, Lukasiuk K (2011) Mechanisms of epileptogenesis and potential treatment targets. Lancet Neurol 10: 173–186. 6. Pernot F, et al. (2011) Inflammatory changes during epileptogenesis and spontaneous seizures in a mouse model of mesiotemporal lobe epilepsy. Epilepsia 52: 2315–2325. 7. Thielsen KD, et al. (2013) The wobbler mouse model of amyotrophic lateral sclerosis (ALS) displays hippocampal hyperexcitability, and reduced number of interneurons, but no presynaptic vesicle release impairments. PLoS One 8:. 8. Ratzliff AH, et al (2002) Mossy cells in epilepsy: Rigor mortis or vigor mortis? Trends Neurosci 25: 140– 144. 9. Scharfman HE, Bernstein HL (2015) Potential implications of a monosynaptic pathway from mossy cells to adult-born granule cells of the dentate gyrus. Front Syst Neurosci 9: 1–16. 10. Sasa M (2006) A New Frontier in Epilepsy: Novel Antiepileptogenic Drugs. J Pharmacol Sci 100: 487–494. 11. Weaver DF (2003) Epileptogenesis, ictogenesis and the design of future antiepileptic drugs. Can J Neurol Sci 30: 4–7. 12. Tatum WO (2012) Mesial temporal lobe epilepsy. J Clin Neurophysiol 29: 356–365. 13. Staley KJ, Dudek FE (2006) Interictal Spikes and Epileptogenesis. Epilepsy Curr 6: 199–202. 14. Pathak D (2017) Paroxysmal Depolarization Shift in Leech Retzius Nerve Cells Revisited. MOJ Anat Physiol 3: 3–5. 15. Debanne D, Thompson SM, Gähwiler BH (2006) A brief period of epileptiform activity strengthens excitatory synapses in the rat hippocampus in vitro. Epilepsia 47: 247–256. 16. Krook-Magnuson E, Soltesz I (2015) Beyond the hammer and the scalpel: Selective circuit control for the epilepsies. Nat Neurosci 18: 331–338. 17. Goldenberg MM (2010) Overview of drugs used for epilepsy and seizures: etiology, diagnosis, and treatment. P T 35: 392–415. 18. Uijl SG, Leijten FSS, Arends JBAM, Parra J, van Huffelen AC, Moons KGM (2008) Decision-making in temporal lobe epilepsy surgery: The contribution of basic non-invasive tests. Seizure 17: 364–373. 19. Spencer S, Huh L (2008) Outcomes of epilepsy surgery in adults and children. Lancet Neurol 7: 525–537. 20. Noachtar S, Borggraefe I (2009) Epilepsy surgery: A critical review. Epilepsy Behav 15: 66–72. 21. Boon P, Raedt R, de Herdt V, Wyckhuys T, Vonck K (2009) Electrical Stimulation for the Treatment of Epilepsy. Neurotherapeutics 6: 218–227. 22. Gröticke I, Hoffmann K, Löscher W (2008) Behavioral alterations in a mouse model of temporal lobe epilepsy induced by intrahippocampal injection of kainate. Exp Neurol 213: 71–83.
49
23. Lévesque M, Avoli M (2013) The kainic acid model of temporal lobe epilepsy. Neurosci Biobehav Rev 37: 2887–2899. 24. Riban V, et al (2002) Evolution of hippocampal epileptic activity during the development of hippocampal sclerosis in a mouse model of temporal lobe epilepsy. Neuroscience 112: 101–111. 25. Löscher W (2002) Animal models of epilepsy for the development of antiepileptogenic and diseasemodifying drugs. A comparison of the pharmacology of kindling and post-status epilepticus models of temporal lobe epilepsy. In, Epilepsy Research pp 105–123. 26. Urban DJ, Roth BL (2015) DREADDs (Designer Receptors Exclusively Activated by Designer Drugs): Chemogenetic Tools with Therapeutic Utility. Annu Rev Pharmacol Toxicol 55: 399–417. 27. Chen X, et al. (2015) The first structure-activity relationship studies for designer receptors exclusively activated by designer drugs. ACS Chem Neurosci 6: 476–484. 28. Roth BL (2016) DREADDs for Neuroscientists. Neuron 89: 683–694. 29. Wojcikiewicz RJH, Tobin AB, Nahorski SR (1993) Desensitization of cell signalling mediated by phosphoinositidase C. Trends Pharmacol Sci 14: 279–285. 30. Gomez JL, et al. (2017) Chemogenetics revealed: DREADD occupancy and activation via converted clozapine. Science (80- ) 357: 503–507. 31. Pirmohamed M, Williams D, Madden S, Templeton E, Park BK (1995) Metabolism and bioactivation of clozapine by human liver in vitro. J Pharmacol Exp Ther 272: 984–990. 32. Raper J, et al. (2017) Metabolism and Distribution of Clozapine-N-oxide: Implications for Nonhuman Primate Chemogenetics. ACS Chem Neurosci 8: 1570–1576. 33. Keswani SG, et al. (2012) Pseudotyped adeno-associated viral vector tropism and transduction efficiencies in murine wound healing. Wound Repair Regen 20: 592–600. 34. Wang X, Zhang C, Szábo G, Sun QQ (2013) Distribution of CaMKIIα expression in the brain in vivo, studied by CaMKIIα-GFP mice1. Wang X, Zhang C, Szábo G, Sun QQ (2013) Distribution of CaMKIIα expression in the brain in vivo, studied by CaMKIIα-GFP mice. Brain Res 1518: 9–25. Brain Res 1518: 9–25. 35. Jones EG, Huntley GW, Benson DL (1994) Alpha calcium/calmodulin-dependent protein kinase II selectively expressed in a subpopulation of excitatory neurons in monkey sensory-motor cortex: comparison with GAD-67 expression. J Neurosci 14: 611–629. 36. Szablowski JO, Lue B, Lee-Gosselin A, Malounda D, Shapiro MiG (2018) Acoustically Targeted Chemogenetics for Noninvasive Control of Neural Circuits. bioRxiv 1–11. 37. Cohen SJ, Stackman RW (2015) Assessing rodent hippocampal involvement in the novel object recognition task. A review. Behav Brain Res 285: 105–117. 38. Vogel-Ciernia A, Wood MA (2014) Examining object location and object recognition memory in mice. Curr Protoc Neurosci 2014: 8.31.1-8.31.17. 39. Vianna MRM (2000) Role of Hippocampal Signaling Pathways in Long-Term Memory Formation of a Nonassociative Learning Task in the Rat. Learn Mem 7: 333–340. 40. Lopez AJ, et al. (2016) Promoter-Specific Effects of DREADD Modulation on Hippocampal Synaptic Plasticity and Memory Formation. J Neurosci 36: 3588–3599. 41. Bender F, et al. (2015) Theta oscillations regulate the speed of locomotion via a hippocampus to lateral septum pathway. Nat Commun 6:. 42. Bannerman DM, et al. (2014) Hippocampal synaptic plasticity, spatial memory and anxiety. Nat Rev Neurosci 15: 181–192. 43. Bannerman DM, et al. (2004) Regional dissociations within the hippocampus - Memory and anxiety. Neurosci Biobehav Rev 28: 273–283. 44. Ben-Shaul Y (2017) OptiMouse: A comprehensive open source program for reliable detection and analysis of mouse body and nose positions. BMC Biol 15:. 45. Levin ED, Christopher NC (2006) Effects of clozapine on memory function in the rat neonatal hippocampal lesion model of schizophrenia. Prog Neuro-Psychopharmacology Biol Psychiatry 30: 223–229. 46. Watson C, Paxinos G (2012) Paxinos and Franklin’s the Mouse Brain in Stereotaxic Coordinates, Fourth Edition. 47. Optimouse I, Ben-shaul Y (2017) OptiMouse User Manual. 48. Twele F, Töllner K, Brandt C, Löscher W (2016) Significant effects of sex, strain, and anesthesia in the intrahippocampal kainate mouse model of mesial temporal lobe epilepsy. Epilepsy Behav 55: 47–56. 49. Duveau V, et al. (2016) Differential Effects of Antiepileptic Drugs on Focal Seizures in the Intrahippocampal Kainate Mouse Model of Mesial Temporal Lobe Epilepsy. CNS Neurosci Ther 22: 497– 506. 50. Twele F, Schidlitzki A, Töllner K, Löscher W (2017) The intrahippocampal kainate mouse model of mesial
50
temporal lobe epilepsy: Lack of electrographic seizure-like events in sham controls. Epilepsia Open 2: 180–187. 51. Bankstahl M, et al. (2016) Knockout of P-glycoprotein does not alter antiepileptic drug efficacy in the intrahippocampal kainate model of mesial temporal lobe epilepsy in mice. Neuropharmacology 109: 183–195. 52. Klee R, Brandt C, Töllner K, Löscher W (2017) Various modifications of the intrahippocampal kainate model of mesial temporal lobe epilepsy in rats fail to resolve the marked rat-to-mouse differences in type and frequency of spontaneous seizures in this model. Epilepsy Behav 68: 129–140. 53. Klein S, Bankstahl M, Löscher W (2015) Inter-individual variation in the effect of antiepileptic drugs in the intrahippocampal kainate model of mesial temporal lobe epilepsy in mice. Neuropharmacology 90: 53– 62. 54. Pearson JN, Schulz KM, Patel M (2014) Specific alterations in the performance of learning and memory tasks in models of chemoconvulsant-induced status epilepticus. Epilepsy Res 108: 1032–1040. 55. Gobbo OL, O’Mara SM (2004) Post-treatment, but not pre-treatment, with the selective cyclooxygenase2 inhibitor celecoxib markedly enhances functional recovery from kainic acid-induced neurodegeneration. Neuroscience 125: 317–327. 56. Hubens C, et al. (2014) Kainate-induced epileptogenesis alters circular hole board learning strategy but not the performance of C57BL/6J mice. Epilepsy Behav 41: 127–135. 57. Chen Z, et al (2002) Excitotoxic neurodegeneration induced by intranasal administration of kainic acid in C57BL/6 mice. Brain Res 931: 135–145. 58. Inostroza M, Cid E, Menendez de la Prida L, Sandi C (2012) Different emotional disturbances in two experimental models of temporal Lobe Epilepsy in rats. PLoS One 7:. 59. Kätzel D, Nicholson E, Schorge S, Walker MC, Kullmann DM (2014) Chemical-genetic attenuation of focal neocortical seizures. Nat Commun 5:. 60. Wicker E, Forcelli PA (2016) Chemogenetic silencing of the midline and intralaminar thalamus blocks amygdala-kindled seizures. Exp Neurol 283: 404–412. 61. Avaliani N, Andersson M, Runegaard AH, Woldbye D, Kokaia M (2016) DREADDs suppress seizure-like activity in a mouse model of pharmacoresistant epileptic brain tissue. Gene Ther 23: 760–766. 62. Forcelli PA (2017) Applications of optogenetic and chemogenetic methods to seizure circuits: Where to go next? J Neurosci Res 95: 2345–2356. 63. Sessolo M, et al. (2015) Parvalbumin-Positive Inhibitory Interneurons Oppose Propagation But Favor Generation of Focal Epileptiform Activity. J Neurosci 35: 9544–9557. 64. Campbell EJ, Marchant NJ (2018) The use of chemogenetics in behavioural neuroscience: receptor variants, targeting approaches and caveats. Br J Pharmacol 175: 994–1003. 65. Mahler S V, Aston-Jones & G (2018) CNO Evil? Considerations for the Use of DREADDs in Behavioral Neuroscience. Neuropsychopharmacology volume 43,: 66. MacLaren DAA, et al. (2016) Clozapine N-Oxide Administration Produces Behavioral Effects in Long-Evans Rats: Implications for Designing DREADD Experiments. eNeuro 3:. 67. Sweeney P, Yang Y (2015) An excitatory ventral hippocampus to lateral septum circuit that suppresses feeding. Nat Commun 6:. 68. Kheirbek MA, et al. (2013) Differential control of learning and anxiety along the dorsoventral axis of the dentate gyrus. Neuron 77: 955–968. 69. Manzaneque JM, Brain PF, Navarro JF (2002) Effect of low doses of clozapine on behaviour of isolated and group-housed male mice in the elevated plus-maze test. Prog Neuro-Psychopharmacology Biol Psychiatry 26: 349–355. 70. Riedel G, et al. (1999) Reversible neural inactivation reveals hippocampal participation in several memory processes. Nat Neurosci 2: 898–905. 71. Liu X, et al. (2012) Optogenetic stimulation of a hippocampal engram activates fear memory recall. Nature 484: 381–385. 72. Zhu H, Pleil KE, Urban DJ, Moy SS, Kash TL, Roth BL (2014) Chemogenetic inactivation of ventral hippocampal glutamatergic neurons disrupts consolidation of contextual fear memory. Neuropsychopharmacology 39: 1880–1892. 73. Mutlu O, Ulak G, Celikyurt IK, Akar FY, Erden F (2011) Effects of olanzapine, sertindole and clozapine on learning and memory in the Morris water maze test in naive and MK-801-treated mice. Pharmacol Biochem Behav 98: 398–404. 74. Keenan WT, Fernandez DC, Shumway LJ, Zhao H, Hattar S (2017) Eye-Drops for Activation of DREADDs. Front Neural Circuits 11:.









