Wat hebben de ziekte van Alzheimer en depressie gemeen?
In mijn masterproef heb ik gezocht naar overeenkomsten en verschillen tussen de ziekte van Alzheimer en depressie. Vraagt u zich af waarom deze schijnbaar totaal verschillende ziektes samen werden onderzocht? Lees dan snel verder!
De ziekte van Alzheimer is de meest gekende vorm van dementie. Verschillende factoren hebben een invloed op de onderliggende biologie en de kans op Alzheimer. Hierbij is ouderdom op zich één van de belangrijkste risicofactoren. Depressie, langs de andere kant, is een veel voorkomende en waarschijnlijk de meest gekende psychiatrische ziekte. Depressie kan zich op veel verschillende manieren uiten. Over de jaren heen zijn verschillende hypotheses naar buiten gebracht over de biologische oorzaak van depressie, maar ook hier is er consensus over een multifactoriële aanleg. Bovendien lijdt een groot deel van de patiënten met Alzheimer ook aan depressie. De laatste jaren is er toenemende aandacht voor neuro-inflammatie in verschillende psychiatrische en neurodegeneratieve ziektes. Bij neuro-inflammatie is er een lage graad van ontsteking in de hersenen, wat een langdurig en nefast effect kan hebben op het functioneren van het brein.
De ziekte van Alzheimer en depressie hebben beide een enorme impact op veel mensen, zowel op de patiënten als hun omgeving. Bovendien is er voor beide aandoeningen momenteel geen medicatie beschikbaar die voor iedereen werkt. Verder stijgt de prevalentie door de veeleisende maatschappij van vandaag en de toenemende vergrijzing. Een belangrijke reden voor het tekort aan medicatie is dat de onderliggende biologie van zowel Alzheimer als depressie nog steeds onvoldoende gekend is. Verder onderzoek blijft dus essentieel. Het wordt echter steeds duidelijker dat er een overlap is in de biologie van verschillende psychiatrische en neurodegeneratieve ziektes zoals depressie en Alzheimer, wat impliceert dat deze aandoeningen beter samen bestudeerd worden en niet elk apart. Dit zou de zoektocht naar gemeenschappelijke behandelingen kunnen bevorderen.
Hoe heb ik dit probleem aangepakt?
In mijn masterproef zocht ik naar gemeenschappelijke en uiteenlopende signaalwegen en hun regulatoren bij Alzheimer en depressie. Een signaalweg is een kettingreactie in de cel van verschillende biomoleculen, waardoor een bepaald proces in gang wordt gezet. Hiervoor werden computationele methoden gebruikt die op basis van beschikbare data voorspellingen maken over biologische signalisatie en interacties. Met deze data werden netwerken gebouwd van verschillende genen die een rol spelen in de ziekte. Deze genen konden zowel regulatoren als hun doelgenen zijn. Regulatoren zijn belangrijke moleculen in onze cellen die mee bepalen welke genen actief worden en welke niet. Deze worden dus als regulatoren gezien van het cellulair netwerk. De doelgenen zijn de genen waarop deze regulatoren werken. Om deze netwerken te construeren werden drie verschillende algoritmen gebruikt. Verschillende methoden kunnen gebruikt worden om netweken te bouwen uit data. Echter, elk van deze methoden heeft zijn voor- en nadelen, waardoor het gunstig is om meerdere methoden te gebruiken. De resultaten van deze algoritmen werden dan samengevoegd tot één collectief netwerk om robuustere resultaten te verkrijgen. Dit werd gedaan voor beide ziektes. Daarnaast werden ook meer precieze data gebruikt, afkomstig van individuele cellen (single-cell) van de hersenen. Hiermee werden ook netwerken geconstrueerd. Zo was het mogelijk om de celtypes die belangrijk zijn voor de ziektes beter te bestuderen. De meest gekende cellen van de hersenen zijn neuronen. Daarnaast zijn er nog andere celtypes, zoals microglia, de immuuncellen van het brein.
De netwerken van de twee ziektes werden dan met elkaar vergeleken om gemeenschappelijke en verschillende signaalwegen en hun regulatoren te vinden. Hiervoor werden clusters van genen, die onder dezelfde omstandigheden actief worden, onderzocht. De functies van de genen binnen eenzelfde cluster werden verder geanalyseerd. Verschillende clusters werden gevonden waar de genen immunologische functies uitvoeren, in zowel Alzheimer als depressie. Het immuunsysteem beschermt normaliter ons lichaam tegen vreemde stoffen. Echter, als het immuunsysteem verkeerdelijk geactiveerd wordt, zorgt dit voor negatieve consequenties en schade in het lichaam. Hoewel in beide ziektes immunologische signaalwegen werden teruggevonden, waren deze niet allemaal identiek aan elkaar. Dit wijst erop dat er slechts een gedeeltelijke overlap is. De regulatoren van deze clusters werden dan verder bestudeerd. Van de meeste regulatoren was reeds geweten dat ze een rol spelen in het immuunsysteem en van enkele was geweten dat ze van belang zijn in microglia. Daarnaast werden er gemeenschappelijke regulatoren gevonden die immunologische clusters in zowel Alzheimer als depressie sturen. Deze waren IKZF1, IRF8, NFATC2, RUNX1 en TAL1.
Deze vijf regulatoren werden verder onderzocht in de netwerken geconstrueerd van de single-cell data. Hier werd gedetecteerd dat deze regulatoren en hun doelgenen allemaal tot expressie komen in de microglia, zowel in Alzheimer als depressie. Deze vijf regulatoren sturen tevens elkaar (zie figuur 1). Eerder onderzoek toonde aan dat alle vijf regulatoren een rol spelen in de biologie van Alzheimer, terwijl enkel TAL1 tot nu toe met depressie geassocieerd is geweest. NFATC2 en IRF8 zorgen voor de activatie van microglia, wat tot neuro-inflammatie kan leiden.
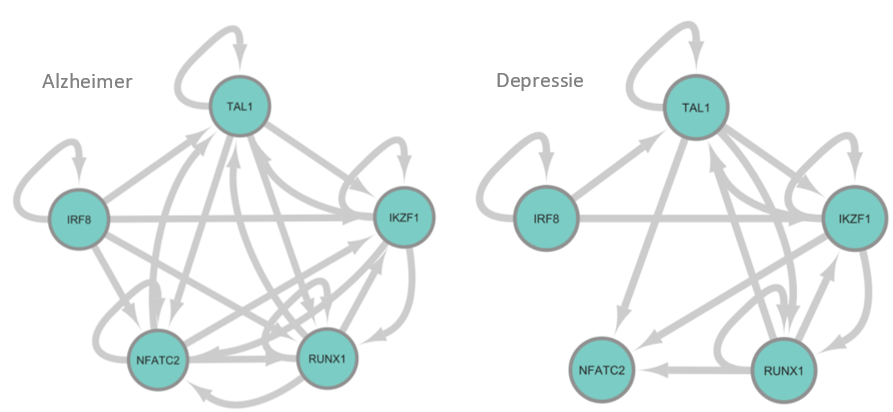 Figuur 1. Netwerken van gemeenschappelijke regulatoren in microglia, betrokken bij immunologische functies. In de blauwe bollen zijn de regulatoren afgebeeld, de pijlen stellen regulatie voor. Links: Alzheimer netwerk, rechts: depressie netwerk, .
Figuur 1. Netwerken van gemeenschappelijke regulatoren in microglia, betrokken bij immunologische functies. In de blauwe bollen zijn de regulatoren afgebeeld, de pijlen stellen regulatie voor. Links: Alzheimer netwerk, rechts: depressie netwerk, .
Naast de immunologische functies werden ook andere signaalwegen ontdekt die gemeenschappelijk zijn tussen de twee ziektes. Ten eerste werd een gestoorde werking van de mitochondria gevonden, wat reeds gekend was in beide ziektes. Dit zorgt ervoor dat de energieproductie van de cellen niet optimaal verloopt. Daarnaast werden genen gevonden die deel uitmaken van het proteasoom in beide netwerken. Het proteasoom is een complex van eiwitten in de cel dat betrokken is bij de afbraak en recyclage van andere eiwitten. Dit was ook reeds geassocieerd met Alzheimer en behandelings-resistente depressie.
Conclusie
Verschillende signaalwegen werden gevonden die ontregeld zijn in Alzheimer en depressie. Er is activatie van microglia, mitochondriale dysfunctie en betrokkenheid van het proteasoom. Verschillende regulatoren werden gevonden die betrokken zijn in de activatie van microglia en disregulatie van het immuunsysteem in beide ziektes. Toekomstig onderzoek is essentieel om hun functie in de biologie van deze ziektes verder te ontrafelen. Daarnaast kunnen deze regulatoren ook gebruikt worden in de zoektocht naar nieuwe medicatie. Biologische netwerken zijn dus een ideale tool om nieuwe invalspunten te vinden voor verschillende ziekten tegelijk.









